常温下,1 mol化学键分解成气态原子所需要的能量用E表示。结合下表信息判断不正确的是
| 共价键 |
H-H |
F-F |
H-F |
H-Cl |
H-I |
| E(kJ·mol -1 ) |
436 |
157 |
568 |
432 |
298 |
A.H2(g)+F2(g)=2HF(g) △H=—25 kJ·mol -1
B.表中最稳定的共价键是H—F键
C.H 2(g)→2H(g) △H=+436 kJ·mol -1
D.432 kJ·mol -1>E(H-Br)>298 kJ·mol -1
下列所列各组物质中,物质之间通过一步反应就能实现如下图所示转化的是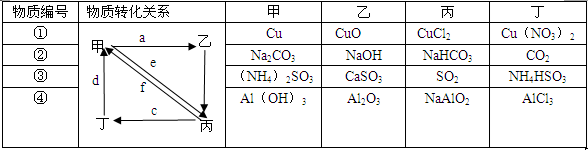
| A.①②③④ | B.①②③ | C.①③④ | D.②④ |
有电子转移的反应一定不是
A.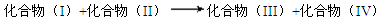 |
| B.反应物总能量大于生成物的总能量的反应 |
| C.同素异形体之间的转化反应 |
| D.相同条件下,同时向正反应方向和逆反应方向进行的反应。 |
著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2。下列说法正确的是
A.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI CeI4 + 2H2↑ CeI4 + 2H2↑ |
| B.在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得Ce |
| C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为Ce4++2Fe2+=Ce3++2Fe3+ |
| D.四种稳定的核素136 58Ce.138 58Ce.140 58Ce.142 58Ce,它们互称为同系物。 |
A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-具有相同的电子层结构,下列叙述一定不正确的是
A.离子半径A2-> C-> B2+ B.它们的原子序数A > B > C
B.它们的原子序数A > B > C
C.它们的原子半径C > B > A D.原子最外层上的电子数C > A > B
铜和镁的合金2.14g完全溶于一定浓度的硝酸,若反应中硝酸被还原为NO2、NO、N2O 三种气体且标准状况下体积均为0.224L,在反应后的溶液中,加入足量的氢氧化钠溶液,生成的沉淀经过滤、洗涤、干燥后称量,质量为
| A.3.12 g | B.4.18 g | C.4.68 g | D.5.08 g |