当光束通过鸡蛋清水溶液时,从侧面观察到一条光亮的“通路”,说明鸡蛋清水溶液是
| A.溶液 | B.胶体 | C.悬浊液 | D.乳浊液 |
关于SO2的叙述中,正确的是()
| A.SO2的摩尔质量是64 g |
| B.常温常压下,64 g SO2中所含的分子数为6.02×1023个 |
| C.1 mol SO2的质量是64 g / mol |
| D.常温常压下,1 mol SO2的体积为22.4 L |
下列各组物质中,前者为混合物,后者为单质的是()
| A.Na2CO3·10H2O Na2CO3 | B.盐酸液氮 |
| C.石油冰 | D.碘酒干冰 |
实验室要用固体氯化钠试剂准确配制0.5 L 、0.2 mol·L-1的NaCl溶液,下列哪种仪器不是必须使用的
| A.500 mL容量瓶 | B.胶头滴管 | C.试管 | D.托盘天平 |
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是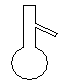

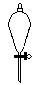
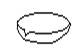
| A.蒸馏、蒸发、分液、过滤 | B.蒸馏、过滤、分液、蒸发 |
| C.分液、过滤、蒸馏、蒸发 | D.过滤、蒸发、分液、蒸馏 |