某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
一、为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 10%过氧化氢溶液与1.0g MnO2均匀混合
Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合
在相同温度下,比较两组实验产生O2的快慢。
(1)为了Ⅰ与Ⅱ中对比x的值应为 。
(2)甲选用下列装置测量产生O2的快慢,正确的是 (填编号)。

二、探究影响双氧水分解速度的某种因素。实验数据记录如下(常温通常指20℃)
| 实验 |
温度 |
药品 |
氧气体积/ml |
反应所需时间/s |
|
| ① |
常 温 |
5% H2O2 |
|
0 |
|
| 常 温 |
5% H2O2 |
MnO2 |
125 |
20 |
|
| ② |
常 温 |
5% H2O2 |
MnO2 |
125 |
20 |
| 热水中 |
5% H2O2 |
MnO2 |
125 |
18 |
|
| ③ |
常 温 |
5% H2O2 |
MnO2 |
125 |
20 |
| 常 温 |
30% H2O2 |
MnO2 |
125 |
5 |
(1)通过实验①对比可知,化学反应快慢与 有关。
(2)通过对比实验 可知,反应物浓度大,反应速率快。
(3)除了上述的两个因素能影响化学反应快慢,你认为另一个影响因素是 ,其关系是 。
(4)由上述实验可知温度、浓度、催化剂等都是影响化学反应速率,实验室用过氧化氢制取氧气的最合适的条件是 。
为了研究炼铁原理,在老师的指导下,同学们在实验室的通风橱内利用下图所示装置(其它实验用品略),进行一氧化碳与氧化铁反应的实验,请你一起参与(每套装置限用一次,可以不用)。
A B C
(1)实验室制得的一氧化碳中常混有二氧化碳和水蒸气,欲用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,正确连接装置导管口的顺序是:混合气体→→g→尾气处理(填导管接口代号)。
(2)装置B中反应的化学方程式。
(3) C实验中玻璃管内观察到的现象为;有关反应的化学方程式为;
(4)本实验停止加热前没有将装置C与D的连接处断开,停止加热后未观察到溶液倒吸现象,请你分析可能的原因是。
(8分)化学实验是学习化学的基础,请根据下列装置图回答问题。

ABC
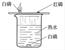
(1) A实验:把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有、和的性质,因此二氧化碳在实际生活中可用于灭火。
(2) B实验:有关反应的化学方程式为;烧杯中热水的作用是使白磷与空气隔绝和;通过该实验可得出燃烧需要三个条件:①可燃物②可燃物与接触③温度达到的结论。
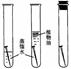
(3) C实验:试管③实验的目的是探究铁钉在的情况下是否生锈;试管①中的铁钉与水面接触的一圈最容易生锈,其原因是___________。
某化学兴趣小组的同学对食品保鲜袋进行了如下研究。
【研究课题】食品保鲜袋的元素组成。
【查阅资料】碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色。
【提出猜想】保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成。
【实验设计】小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成。
【实验步骤】
(1)按上图图示连接好仪器。
(2)检查装置的气密性。
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装。
(4)向A中缓慢注水一段时间后,将已称重的D、E两干燥管和未称重的F干燥管接到C的尾端。
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧。
(6)熄灭酒精灯并继续向A中注水一段时间。
(7)分别对D、E进行第2次称重。
【实验分析】
(1)B处的浓硫酸的作用是。F处干燥管的作用是。
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了。
(3)熄灭酒精灯后继续向A中注水一段时间是为了。
【实验结论】第1次对D、E称重质量分别为(此处缺少数据);第2次对D、E称重质量分别为(此处缺少数据),则该食品保鲜袋的元素组成为。(本小题无法解答)
某兴趣小组的同学利用下图装置研究二氧化碳的性质。(仪器的固定装置已经省略)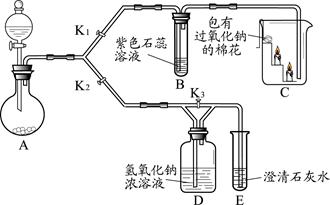
(1)A装置用于实验室制取二氧化碳,其反应的化学方程式为。
(2)实验开始后,关闭K2、打开K1,可观察到B中现象为;C中的蜡烛由下至上依次熄灭,说明二氧化碳具有的性质是;待蜡烛熄灭后,铁片上的棉花剧烈燃烧起来,由此可得到的推论是。
(3) 实验开始后,关闭K1和K3,打开K2,观察E中现象,然后打开K3,再观察E中现象,其不同之处是,有关反应的方程式为。
某学校化学学习小组同学设计出下图所示装置,并进行白磷燃烧实验。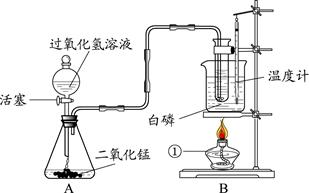
(1)图中标“①”的仪器名称是。
(2)图A可用于实验室制氧气,其反应的化学方程式为,氧气的收集方法是或。
(3)当烧杯内的水受热,温度计显示30℃时,打开图A中分液漏斗的玻璃塞和活塞,在图B中盛有水的试管中有气泡均匀逸出,白磷未燃烧,白磷未燃烧的原因是。
(4)随着水温升高,温度计显示40℃时,再次打开活塞,白磷在水里燃烧。白磷燃烧的化学方程式为。