如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22,下列说法正确的是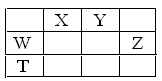
| A.X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B.由X、Y和氢三种元素形成的化合物中只有共价键 |
| C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 |
| D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
某无色溶液,由Na+、K+、Ag+、Ba2+、Al3+、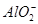 、
、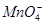 、
、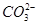 、
、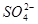 中的若干种组成。取该溶液进行如下实验:(1)取适量溶液,加入过量盐酸,有气体生成,并得到溶液;(2)在(1)所得溶液中加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;(3)在(2)所得溶液中加入过量氢氧化钡溶液,微热,也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定存在的是()
中的若干种组成。取该溶液进行如下实验:(1)取适量溶液,加入过量盐酸,有气体生成,并得到溶液;(2)在(1)所得溶液中加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;(3)在(2)所得溶液中加入过量氢氧化钡溶液,微热,也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定存在的是()
| A.Na+ | B.Al3+ | C.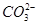 |
D.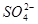 |
常温下,将0.1 mol·L-1盐酸和0.06 mol·L-1氢氧化钡溶液等体积混合后,该混合溶液的pH是()
| A.1.7 | B.12.3 | C.12 | D.2 |
用物质的量都是0.1 mol的HCN和NaCN混合后配成1 L溶液,已知溶液中的c(CN-)<c(Na+),下列关系式正确的是()
| A.c(H+)>c(OH-) | B.c(HCN)>c(CN-) |
| C.c(CN-)+c(OH-)="0.1" mol·L-1 | D.c(HCN)+c(CN-)="0.1" mol·L-1 |
常温时,将V1 mL c1 mol·L-1的氨水滴加到V2 mL c2 mol·L-1的盐酸中,下列结论中正确的是()
| A.若混合溶液的pH=7,则c1V1=c2V2 |
B.若V1=V2,c1=c2,则混合液中c(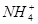 )=c(Cl-) )=c(Cl-) |
C.若混合液的pH=7,则混合液中c(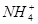 )=c(Cl-) )=c(Cl-) |
| D.若V1=V2,且混合液的pH<7,则一定有c1<c2 |
对室温下pH相同,体积相同的盐酸和醋酸两种溶液分别采取下列措施,有关叙述一定正确的是()
| A.加水稀释3倍后,两溶液pH仍然相同 |
| B.加入CH3COONa晶体后,两溶液pH均增大 |
| C.加入足量的苏打固体充分反应后,两溶液中产生的CO2一样多 |
| D.分别加入足量的锌粉充分反应,反应自始至终两酸产生H2的反应速率相等 |