可逆反应:aA(g)+bB(s) cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是
cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是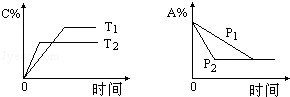
| A.T1<T2 △H>0 | B.T1>T2 △H<0 |
| C.P1<P2a="c+d" | D.P1<P2 a+b=c+d |
有关纯碱和小苏打的叙述正确的是
| A.等质量的Na2CO3、NaHCO3分别与足量稀H2SO4反应,NaHCO3产生的CO2多 |
| B.等质量的Na2CO3、NaHCO3分别与足量的同种盐酸反应,NaHCO3消耗的盐酸多 |
| C.向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀 |
| D.Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠反应 |
氮化铝(AlN)广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:Al2O3+N2+3C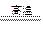 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
| A.上述反应中,N2是还原剂,Al2O3是氧化剂 |
| B.上述反应中,每生成1 mol AlN需转移3 mol电子 |
| C.AlN的摩尔质量为41 g |
| D.AlN中氮的化合价为+3 |
以下物质的制备原理错误的是
A.无水氯化镁的制备:MgCl2·6H2O MgCl2+6H2O MgCl2+6H2O |
B.钴的制备:3Co3O4+8Al 9Co+4Al2O3 9Co+4Al2O3 |
C.烧碱的制备:2NaCl+2H2O 2NaOH +H2↑+ Cl2↑ 2NaOH +H2↑+ Cl2↑ |
D.漂粉精的制备: 2Ca(OH) 2 + 2Cl2 Ca(ClO) 2 +CaCl2+2H2O Ca(ClO) 2 +CaCl2+2H2O |
NA表示阿伏伽德罗常数,下列判断正确的是
| A.1mol Na2O2固体中含离子总数为4 NA |
| B.1 molCl2参加反应转移电子数一定为2 NA |
| C.常温下,1L 1mol/L的NH4NO3溶液中氮原子数为0.2 NA |
| D.标准状况下,2.24L戊烷所含分子数为0.1 NA |
冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或氢气,或一氧化碳)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁,对它们的冶炼方法的分析不正确的是
| A.(Ⅰ)用① | B.(Ⅱ)用② |
| C.(Ⅲ)用③ | D.(Ⅳ)用④ |