甲醇的研究成为当代社会的热点.
Ⅰ.甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
(1)101kP 时,1mol CH3OH完全燃烧生成稳定的氧化物放出热量726.51kJ/mol,则甲醇燃烧的热化学方程式为__________.
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol﹣1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g)△H2
O2(g)=CO2(g)+2H2(g)△H2
已知H2(g)+ O2(g)=H2O(g)△H=﹣241.8kJ•mol﹣1
O2(g)=H2O(g)△H=﹣241.8kJ•mol﹣1
则反应②的△H2=__________.
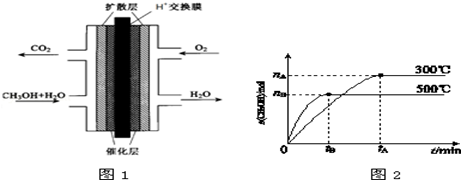
(3)甲醇燃料电池的结构示意图如图1.负极发生的电极反应为____________________.
Ⅱ.一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)⇌CH3OH(g)达到化学平衡状态.
(1)根据图2,纵坐标为CH3OH的物质的量,升高温度,K值将__________(填“增大”、“减小”或“不变”).
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是__________(用nB、tB表示).
(3)判断该可逆反应达到化学平衡状态的标志是__________(填字母).
a.CO、H2、CH3OH的浓度均不再变化
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.v生成(CH3OH)=v消耗(CO)
e.混合气中n(CO):n(H2):n(CH3OH)=1:2:1
(4)300℃时,将容器的容积压缩到原来的 ,在其他条件不变的情况下,对平衡体系产生的影响是__________(填字母).
,在其他条件不变的情况下,对平衡体系产生的影响是__________(填字母).
a.c(H2)减少 b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加 d.重新平衡时 减小.
减小.
下表所列物质(括号内为少量杂质),在B中选择试剂,在C中选择操作的方法。填表(填入序号):
B:(1)CaO;(2)NaOH溶液;(3)溴水; (4)饱和Na2CO3;(5)水
C:(1)重结晶;(2)洗气;(3)蒸馏(4)分液。
| 物质 |
加入试剂 |
操作方法 |
| ①粗苯甲酸的提纯 |
▲ |
▲ |
| ②乙醇(水) |
▲ |
▲ |
| ③乙酸乙酯(乙酸) |
▲ |
▲ |
| ④乙烷(乙烯) |
▲ |
▲ |
| ⑤苯(酒精) |
▲ |
▲ |
某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过过量的浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。实践中可根据核磁共振氢谱(NMR)上观察到氢原子给出的峰值情况,确定有机物的结构。此含有苯环的有机物,在NMR谱上峰给出的稳定强度仅有四种,它们分别为:① 3∶1∶1 ②1∶1∶2 ∶6 ③3∶2 ④3∶2∶2∶2∶1 ,(1)由以上信息得出该有机物的分子式为_▲_;
(2)请分别推断出③④对应物质的结构简式:③▲; ④▲ 。
实验测定某有机物元素质量组成为C:69%,H:4.6%,N:8.0%,其余是O,相对分子质量在300~400之间,则该有机物的实验式为▲_,相对分子质量为▲_,分子式为▲_。
已知某有机物的结构简式为: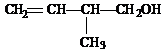
(1)该有机物中所含官能团的名称是_▲_、_▲_。
(2)该有机物发生加成聚合反应后,所得产物的结构简式为_▲_。
(3)写出该有机物与乙酸的酯化反应的化学方程式(注明反应条件):_▲_
(1)双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。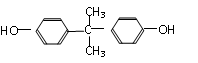
双酚A的核磁共振氢谱显示氢原子数之比是▲
(2)对羟基扁桃酸是农药、药物、香料合成的重要中间体, 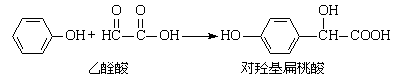
在核磁共振氢谱中对羟基扁桃酸应该有▲吸收峰