将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s) NH3(g)+HI(g) ②2HI(g)
NH3(g)+HI(g) ②2HI(g) H2(g)+I2(g) 达到平衡时,c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,,则此温度下反应①的平衡常数为
H2(g)+I2(g) 达到平衡时,c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,,则此温度下反应①的平衡常数为
| A.9 | B.16 | C.20 | D.25 |
空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”建设的是
| A.推广使用燃煤脱硫技术,防治SO2污染 |
| B.实施绿化工程,防治扬尘污染 |
| C.研制开发燃料电池汽车,消除机动车尾气污染 |
| D.加大石油、煤炭的开采速度,增加化石燃料的供应量 |
中和滴定是一种操作简单,准确度高的定量分析方法。实际工作中也可利用物质间的氧化还原反应、沉淀反应进行类似的滴定分析,这些滴定分析均需要通过指示剂来确定滴定终点,下列对几种具体的滴定分析(待测液置于锥形瓶内)中所用指示剂及滴定终点时的溶液颜色的判断不正确的是( )
| A.用标准酸性KMnO4溶液滴定Na2SO3溶液以测量其浓度:KMnO4——紫红色 |
| B.利用“Ag++SCN-===AgSCN↓”原理,可用标准KSCN溶液测量AgNO3溶液浓度:Fe(NO3)3——红色 |
C.利用“2Fe3++2I-===I2+2Fe2+”, 用FeCl3溶液测量KI样品中KI的百分含量: 用FeCl3溶液测量KI样品中KI的百分含量:淀粉——蓝色 |
| D.利用OH-+H+===H2O来测量某盐酸溶液的浓度时:酚酞——浅红色 |
为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是( )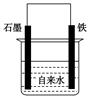
| A.正极的电极方程式为:O2+2H2O+4e-===4OH- |
| B.将石墨电极改成Mg电极,难以观察到铁锈生成 |
| C.若向自来水中加入少量NaCl(s),可较快地看到铁锈 |
| D.向铁电极附近吹入O2比向石墨电极附近吹入O2,铁锈出现得快 |
欲使0.1 mol·L-1的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减小,其方法是( )
| A.通入CO2 |
| B.加入NaOH固体 |
| C.通入HCl |
| D.加入饱和石灰水溶液 |
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是( )
| A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动 |
| B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为: Al-3e-+4OH-===AlO2-+2H2O |
| C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-===Cu2+ |
| D.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗铜电极32 g |