现用Zn与实验室中的盐酸反应制取4.48L H2(标准状况)。
(1)求消耗得锌的质量为多少克?
(2)如果选用所贴标签为2.0mol·L-1的盐酸,至少需该盐酸多少毫升?
(3)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升?(Zn+2HCl = ZnCl2+H2)
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)煤的气化的主要化学反应方程式为:_______________________。
(2)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g)+ CO(g)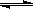 CH3OH(g);ΔH=-9
CH3OH(g);ΔH=-9 0.8 kJ·mol-1
0.8 kJ·mol-1
② 2CH3OH(g)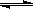 CH3OCH3(g)+H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g)+H2O(g)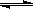 CO2(g)+ H2(g);ΔH=-41.3 kJ·mol-1
CO2(g)+ H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g)+ 3CO(g)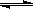 CH3OCH3(g)+CO2 (g)的ΔH=___________;
CH3OCH3(g)+CO2 (g)的ΔH=___________;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压 b.加入催化剂c.减少CO2的浓度
b.加入催化剂c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(3)已知反应②2CH3OH(g) CH3OCH3(g)+H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器 中加入CH3OH,反应到某时刻测得各组分的浓度如下:
中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
①比较此时正、逆反应速率的大小: v正______ v逆 (填“>”、“<”或“=”)。
v正______ v逆 (填“>”、“<”或“=”)。
②若加入CH3OH后,经10 min 反应达到平衡,此时c(CH3OH) =_________;该时间内反应速率v(CH3OH) =__________。
反应达到平衡,此时c(CH3OH) =_________;该时间内反应速率v(CH3OH) =__________。
在25℃、101kPa条件下,将15L O2通往10L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气体中,V(CO)=L,V(H2)=L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气中,V(CO): V(H2)=。
(3)若剩余气体的体积为a L,则a的取值范围如何表示?写出此问的计算过程。
2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液处理,发生反应如下: +5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O +5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
______ +______Fe2++______H+=______Mn2++______Fe3++______H2O
+______Fe2++______H+=______Mn2++______Fe3++______H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为________mol。
(3)欲配制500 mL 0.1 mol·L-1 Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M="392" g·mol-1)的质量为________g。
(4)混合物中Cu2S的质量分数为_______。
将过量Mg粉溶于100mL 1.5mol·L-1稀H2SO4中,反应结束后,滤去多余Mg粉,滤液在t℃下蒸发,当滤液质量为72.0g时开始析出MgSO4·xH2O晶体,当析出晶体12.3g时,剩下滤液48 .0g。通过计算请回答下列问题(请写出计算过程)。
.0g。通过计算请回答下列问题(请写出计算过程)。
(1)生成标准状况下 的气体体积;
的气体体积;
( 2)开始析出MgSO4·xH2O晶体时溶液的质量分数;
2)开始析出MgSO4·xH2O晶体时溶液的质量分数;
(3)MgSO4·xH2O中的x值。
红磷 P (s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g)。如图所示(图中的△H表示生成 l mol 产物的数据)。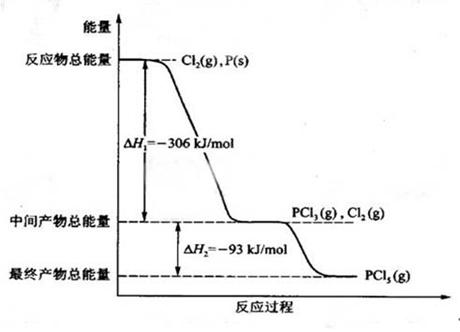
根据上图回答下列问题:
(1)P和CI2反应生成 PC13的热化学方程式是______________________________;
(2)PC15分解成 PC13和 Cl2的热化学方程式是_____________________________;上述分解反应是一个可逆反应。温度 Tl时,在密闭容器中加人 0.80 mol PC15,反应达平衡时 PC15还剩 0.60 mol ,其分解率 al等于_________________;若反应温度由 Tl升高到T2,平衡时 PC15的分解率为a2,a2_________ al(填“大于”、“小于”或“等于”) ;
(3)工业上制备 PC15通常分两步进行,先将 P 和 C12反应生成中间产物 PC13,然后降温,再和Cl2反应生成 PCl5。原因是___________________________________
______________________________________________________;
(4)P 和 C12分两步反应生成 1 mol PC15的△H3==__________________,一步反应生成 1 molPC15的△H4____________△H3(填“大于”、“小于”或“等于”)。
(5)PC15与足量水充分反应,最终生成两种酸,其化学方程式是
______________________________________________________________________。