暗紫色固体A在加热的条件下反应生成B和C以及D,常温下过氧化氢溶液遇到C时分解放出D,其中C在反应前后的质量和化学性质都没有改变,若将细铁丝放在D中点燃能剧烈燃烧,火星四射,生成黑色固体E。
(1)写出各物质的名称:
A ;B ;C ;D ;E
(2)用文字表达式表示有关的化学反应,并指出反应所属的类型(化合反应、分解反应):
① ( );
② ( );
③ ( )。
A、B、C、D、E分别代表氧化铜、稀硫酸、氢氧化钡溶液、碳酸钾溶液、铁丝五种物质中的某一种,相交的两个圊内的物质能够发生反应一其中C为草木灰的主要成分,A、E反应溶液颜色有变化.
(1)请在D、E的周围画出A、B、C三个圆,以表示各物质之间的反应,并标明物质的化学式.
(2)写出产生白色沉淀的化学方程式:
(3)D与E反应的现象:.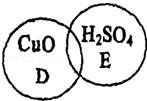
现有A、B、C、D四种物质分别是稀盐酸、氢氧化钠溶液、铁粉、硝酸银溶液,用四个圆形表示A(铁粉)、B(稀盐酸)、C(硝酸银溶液)、D(氢氧化钠溶液)四种物质,用相邻的圆形相切表示两种物质可以发生反应,请回答下列问题:
(1)用两个圆形表示C、D两种物质,将C、D两个圆形画到图中A、B周围适当的位置,并在圆形中写出物质名称;
(2)写出产生气体的化学方程式;
(3)A与C反应的实验现象为.
有A、B、C、D四种元素,已知A是地壳中含量最多的元素,B元素的原子失去一个电子后只剩下一个质子,C元素是海水中含量最高的金属元素,D2-的电子层结构与氩原子相同。请回答:A元素的名称或符号;B元素的离子符号;C元素组成单质的化学式;A、C、D元素组成化合物的化学式。
下列图示是城市污水处理流程图:
阅读流程图,回答下列问题:
(1)在污水处理流程中,一级处理过程中使用的处理方法属于变化.
(2)在消毒清水池中常用二氧化氯这种物质对水进行消毒,二氧化氯的化学式是,其中氯元素的化合价是。
(3)经过二级处理的水称为中水,可回用于城市用水,其标准之一是水中含有铁≤0.3,这里的铁指的是铁。
(4)该污水处理流程中,活性炭的作用是。
(5)日常生活中你经常采用的节水措施有.
现有A、B、C、D四种物质,其中A、B常温下都是一种无色液体,它们具有相同的组成元素,C、D为常见的无色气体。一定条件下四种物质存在下图所示的转化关系:
请根据以上事实回答下列问题:
(1)写出有关物质的化学式:A, B。
(2)写出反应②的文字表达式或化学方程式:,基本反应类型______反应,
写出反应③的文字表达式或化学方程式:。