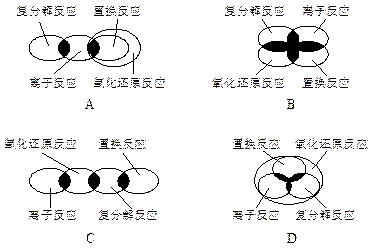工业用CO生成生成甲醇的反应为CO(g)+2H2(g) ⇌CH3OH(g) △H =" a" kj/mol图1表示反应中能量的变化;图2表示一定温度下,在体积固定为1L的密闭容器中加入2mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图.下列叙述错误的是
| A.CO和H2合成CH3OH的反应:△H<0,△S<0 |
| B.保持温度不变,再充入1molCO和2molH2,反应达到新平衡时n(CH3OH)/n(CO)减小 |
| C.图1中曲线b可表示使用了催化剂的能量变化情况 |
| D.图3中曲线可表示在不同压强P1、P2(P1<P2)条件下甲醇百分含量随温度变化的情况 |
关于硫的叙述正确的是
| A.硫的非金属性较强,所以只以化合态存在于自然界 |
| B.分离黑火药中的硝酸钾、炭、硫要用到二硫化碳、水以及过滤操作 |
| C.硫与金属或非金属反应均作为氧化剂 |
| D.1.6 g硫与6.4 g铜反应能得到8.0 g纯净硫化物 |
为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入
| A.水;无水CaCl2固体 |
| B.饱和NaHCO3溶液;浓H2SO4 |
| C.浓H2SO4;饱和Na2CO3溶液 |
| D.饱和Na2CO3溶液;稀H2SO4 |
用石灰水保存鲜蛋是一种化学保鲜方法,这种保存鲜蛋方法的原理是
①石灰具有强碱性,杀菌能力强②Ca(OH)2能与鲜蛋呼出的CO2反应,生成碳酸钙薄膜,起保护作用③石灰水是电解质溶液,能使蛋白质凝聚④石灰水能渗入蛋内中和酸性物
| A.①② | B.①③ |
| C.②③ | D.③④ |
向下列物质①大理石,②钟乳石,③锅垢,④贝壳,⑤蛋壳,分别滴加醋酸,会产生相同气体的
| A.只有①② |
| B.只有④⑤ |
| C.只有①②③ |
| D.是①②③④⑤ |
离子反应、复分解反应、置换反应和氧化还原反应之间可用集合关系表示,其正确的是