已知25℃时有关弱电解质的电离平衡常数如下表:
| 弱电解质化学式 |
CH3COOH |
HCN |
H2CO3 |
NH3.H2O |
| 电离平衡常数 |
1.8×l0–5 |
4.9×l0–10 |
K1=4.3×l0–7 K2=5.6×l0–11 |
1.8×l0–5 |
根据上表中数据回答下列问题:
(1)CH3COO-、CN-、CO32-结合质子(即H+)的能力大小顺序__________________;25℃时,有等浓度的①CH3COONa溶液、②NaCN溶液、③NaHCO3溶液,三种溶液的pH由大到小的顺序为 (填序号)。
(2)NaCN溶液中通入少量二氧化碳,反应的离子方程式为
(3)向稀氨水中加入等体积等浓度的醋酸溶液,则反应后溶液中各离子浓度大小关系为
(4)甲、乙两瓶氨水的浓度分别为1mol·L-1、0.1mol·L-1,则c(OH-)甲﹕c(OH-)乙 10(填“>”、“=”或“<”)。
研究碳及其化合物的综合利用对促进低碳社会的构建具有重要的意义。请运用相关知识研究碳及其化合物的性质。
(1)近年来,我国用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
C+K2Cr2O7+ —CO2↑+ K2SO4 + Cr2(SO4)3+H2O
①完成并配平上述化学方程式。
②在上述方程式上用单线桥标出该反应电子转移的方向与数目。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是。
②由MgO可制成“镁-次氯酸盐”电池,其装置示意图如图1,该电池反应的离子方程式为。 
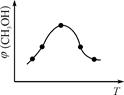

图1图2图3
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g) +3H2(g) CH3OH(g) +H2O(g)△H
CH3OH(g) +H2O(g)△H
①该反应的平衡常数表达式为K=。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的△H0(填“>”“<”或“=”)。
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、II对应的平衡常数大小关系为KⅠKII(填“>” “<”或“=”)。
有机物W~H 有如下的转化关系。已知W、B为芳香族化合物,X为卤素原子,W、A、B均能与NaHCO3溶液反应,A分子中有2个甲基,H分子中含有醛基且苯环上的取代基处于对位。
已知:
请回答下列有关问题:
(1)反应①属于 反应(填有机反应类型),A、B中均含有的含氧官能团的名称是 。
(2)F的化学式,B的结构简式。
(3)反应②的化学方程式是。
(4)若 ,反应④的化学方程式是 。
,反应④的化学方程式是 。
(5)H有多种同分异构体,且满足下列3个条件
(i)遇FeCl3显紫色
(ii)苯环上一取代物有两种
(ⅲ)除苯环外无其它环状结构
请任意写出1种符合条件的物质的结构简式______________________;
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物。
(1)下列叙述正确的是。(填字母)
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个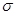 键和1个大
键和1个大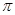 键,C6H6是非极性分子
键,C6H6是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
| 元素 |
Mn |
Fe |
|
| 电离能 /kJ·mol-1 |
I1 |
717 |
759 |
| I2 |
1509 |
1561 |
|
| I3 |
3248 |
2957 |
Mn元素价电子排布式为,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是。
(3)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Ti属于 区。
(4)Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为。
(5)电镀厂排放的废水中常含有剧毒的CN-离子,可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
①H、C、N、O四种元素的电负性由小到大的顺序为。
②与CNO-互为等电子体微粒的化学式为(写出一种即可)。
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
某工厂以天然气、水蒸气和空气为原料和能源合成氨的流程如右图:
该流程中外热式一级烃转化器系指以 CH4为燃料在烃气转化器外面加热使之维持 8000C高温的工业装置。内热式一级烃气转化器系指以H2在装置内燃烧为能量维护一级烃气转化器所生成的CO与H2O(g)反应生成CO2和H2所需10000C高温的装置。在编号为i-v的反应器中发生如下反应:
| A.CH4+2O2=CO2 +2H2O | B.CH4+H2O(g)=CO +3H2 |
| C.2CH4+3H2O(g)=CO + CO2 +7H2 | D.K2CO3+CO2 +H2O=2KHCO3 |
E.CO+ H2O(g) CO2 + H2ΔH<0 F.2H2 +O2=2H2O
CO2 + H2ΔH<0 F.2H2 +O2=2H2O
(1)反应A发生在编号为______的反应器中,它的作用是_______________________________。
(2)反应F发生在编号为____________的反应器中。
(3)反应D的作用是____________。
(4)属于制备合成氨原料气的反应有______(填化学方程式编号)。
(5)为什么转化反应要分两步——第一步在4000C时进行,第二步在200 0C时进行?
________________________________________________________________________________。
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g) FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。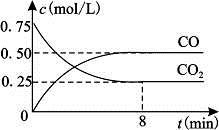
(1)下列措施中能使平衡时K增大的是___________(填序号);
A.升高温度 B.增大压强C.充入一定量COD.降低温度
(2)8分钟内,CO的平均反应速率v(CO)=___________mol/(L·min);
(3)1100℃时,2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
| 容器 |
甲 |
乙 |
| 反应物投入量 |
3molFe、2molCO2 |
4molFeO、3molCO |
| CO的浓度(mol/L) |
C1 |
C2 |
| CO2的体积分数 |
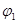 |
 |
| 体系压强(Pa) |
P1 |
P2 |
| 气态反应物的转化率 |
 |
 |
①下列说法正确的是___________;
A. B.
B.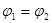 C.P1<P2D.
C.P1<P2D.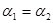
②求 =___________、
=___________、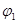 =___________、
=___________、 =___________。
=___________。