某化学探究小组拟用废铜屑制取Cu(NO3)2并探究其化学性质。
I、如右图所示,用浓HNO3和过量的废铜屑充分反应制硝酸铜溶液。

(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤依次是:蒸发浓缩、 、过滤、 、烘干。
③你认为此装置是否合理,并说明原因 。
Ⅱ、为了探究Cu(NO3)2热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)

(3)往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;在集气瓶中收集到无色气体。由此判断Cu(NO3)2受热分解的化学方程式为 。
Ⅲ、利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。下表是化学探究小组的实验记录,据此回答相关问题:
| 实验序号 |
1 |
2 |
3 |
4 |
| 温度/℃ |
35 |
50 |
70 |
95 |
| 样品颜色 |
深蓝色 |
深蓝色 |
浅绿色 |
暗蓝色 |
(4)95℃时,制得的样品颜色发暗的可能原因是: 。
(5)70℃时,实验得到3.82 g样品,取此样品加热至分解完全(杂质不反应),得到3.20 g固体,此样品中碱式碳酸铜的质量分数是 。
利用硫酸厂烧渣(含铁的氧化物和少量FeS及SiO2)制碱式硫酸铁的流程如下:
(1)SO2与过量NaOH溶液反应的离子方程式为。
(2)滤渣的主要成分为(填化学式)。
(3)反应1中加双氧水的目的是。
(4)碱式硫酸铁的化学式为Fex(OH)y(SO4)z·nH2O,为确定其组成进行如下实验:
①称取1.6920 g 样品溶于足量的稀盐酸中;
②加足量的BaCl2溶液,过滤、洗涤、干燥、称重,得固体质量为2.3300 g;
③向步骤②的滤液中加过量的NaOH溶液,过滤、洗涤、灼烧、称重,得固体质量为0.6400 g。
根据以上实验数据计算碱式硫酸铁样品中的n(OH-): n(SO42-)(写出计算过程)
(10分)镁铝合金在交通、航空、电子等行业有着广泛的应用。某化学兴趣小组试对镁铝合金废料进行回收利用,实验中可将铝转化为硫酸铝晶体,并对硫酸铝晶体进行热重分析。镁铝合金废料转化为硫酸铝晶体实验流程如下: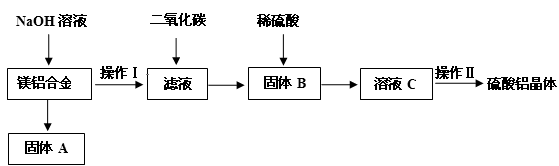
试回答下列问题:
(1)在镁铝合金中加入NaOH溶液,写出反应的化学反应方程式,固体B的化学式。
(2)操作Ⅱ包含的实验步骤有:蒸发浓缩、、、洗涤、干燥。
(3)操作Ⅱ中常用无水乙醇对晶体进行洗涤,选用无水乙醇的原因是。
(4)若初始时称取的镁铝合金废料的质量为9.00 g,得到固体A的质量为4.95 g,硫酸铝晶体的质量为49.95 g(假设每一步的转化率均为100%,合金废料中不含溶于碱的杂质)。计算得硫酸铝晶体的化学式为。
(5)取上述硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:323K-523K,553K-687K,1043K以上不再失重,其热分解的TG曲线见下图,
已知: 。
。
根据图示数据计算确定每步分解的产物,写出第一阶段分解产物的化学式,第三阶段反应化学方程式。
用中各滴定法测定某烧碱样品的纯度,若烧碱中含有不反应的杂质,试根据实验回答:
(1)将准确称好的5.0 g烧碱样品配成250 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、胶头滴管处,还必须用到的玻璃仪器有________。
(2)取待测液10.00 mL,需用________(填仪器名称)量取,并置于锥形瓶中。
(3)向锥形瓶中滴加两滴指示剂,用0.200 mol/L HCl溶液滴定烧碱溶液。不适宜选用的指示剂为(选序号填):________。
①石蕊溶液②酚酞溶液 ③甲基橙溶液
(4)滴定操作的要领是:左手握活塞,右手摇锥形瓶,眼睛要注视________。
(5)根据下表实验数据,可计算出烧碱的纯度为________。
| 滴定次数 |
待测液体积(mL) |
HCl溶液体积(mL) |
|
| 滴定前读数 |
滴定后读数 |
||
| 第一次 |
10.00 |
0.50 |
20.51 |
| 第二次 |
10.00 |
4.00 |
24.00 |
| 第三次 |
10.00 |
5.11 |
25.10 |
(6)下列操作会使所测溶液的浓度数值偏高的是(填代号)________。
A.酸式滴定管未用HCl溶液润洗就直接注入HCl溶液
B.锥形瓶用蒸馏水洗净后没有干燥就注入NaOH待测液
C.装有HCl溶液的酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取HCl溶液体积时,开始仰视读数,滴定结束后俯视读数
(10分)根据下图所示实验回答下列问题:
(l)试管A中发生反应的化学方程式是___________________________________________
试管C口部的棉团中发生反应的离子方程式是_______________________________
(2)试管B中的实验现象是______________________________________
若将该试管中反应后的溶液加热,可以观察到试管B中的实验现象是__________________
通过试管C中的实验现象,可以证明SO2是氧化物。(填“酸性”,“碱性”或“两性” )
(16分)实验室用氯化钠固体配制1.0 mol/L的NaCl溶液500 mL,回答下列问题:
(1)所需仪器为:容量瓶(规格为________)、托盘天平,还需要哪些实验仪器才能完成该实验,请写出: ________________
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用托盘天平准确称取所需NaCl的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其溶解均匀
C.将已冷却的溶液注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)下列操作对所配溶液的浓度有何影响?(填写字母)偏小的有____________,偏大的有_______,无影响的有_______________________
A.称量时使用了生锈的砝码
B.往容量瓶中移液时,有少量液体溅出
C.定容时仰视刻度线
D.容量瓶未干燥即用来配制溶液
(4)溶液注入容量瓶前需恢复到室温,这是因为;
(5)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度;