下列关于物质的量浓度表述正确的是
A.0.2mol·L-1Na2SO4溶液中含有Na+和SO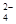 总物质的量为0.6mol 总物质的量为0.6mol |
| B.50mL2mol·L-1NaCl溶液和100mL0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等 |
| C.用1L水吸收22.4L氯化氢所得盐酸的浓度是1mol·L-1 |
| D.10g98%的硫酸(密度为1.84g·cm-3)与10mL18.4mol·L-1的硫酸的浓度是相同的 |
在物质分类中,前者 包括后者的是()
包括后者的是()
| A.氧化物、化合物 | B.溶液、胶体 |
| C.电解质、化合物 | D.分散系、溶液 |
下面是人们对于化学科学的各种常见认识,其中错误的是()
| A.化学是一门以实验为基础的自然科学 |
| B.化学是一门具有较强实用性的科学 |
| C.化学支持高新技术的快速发展,但面对伪科学和人体健康等问题却显得无能为力 |
| D.化学将为解决能源问题、环境问题、资源问题等提供有效途径和方法 |
C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2。将2.00 g C跟16.0 g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是
| A.反应后的固体混合物中单质Cu的质量为12.8 g |
| B.反应后的固体混合物中还含有碳 |
| C.反应后的固体混合物总质量为14.4 g |
| D.反应后的固体混合物中氧化物的物质的量为0.05 mol |
将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g) + Y(g)  2Z(g);△H < 0。当改变某一条件并达到新平衡后,下列叙述正确的是
2Z(g);△H < 0。当改变某一条件并达到新平衡后,下列叙述正确的是
| A.缩小容器体积,Z的浓度不变 |
| B.升高温度,X的转化率增大 |
| C.保持容器体积不变,充入一定量的氦气,Y的浓度不变 |
| D.保持压强不变,再充入0.2 mol X和0.2 mol Y,X的体积分数增大 |
下列结论错误的是
①离子的还原性:S2– > Cl– > Br– > I–;②酸性:H2SO4 > H3PO4 > H2CO3 > HClO;
③微粒半径:K+ > Al3+ > S2– > Cl–;④氢化物的稳定性:HF > HCl > H2S > PH3 > SiH4;
⑤物质的熔沸点:金刚石 > NaCl > H2O > H2Se > H2S。
| A.只有① | B.①③ | C.①③⑤ | D.②④⑤ |