短周期主族元素X、Y、Z、W原子序数依次增大,X与Z原子序数相差8, Y元素的焰色为黄色,Z元素的最高价为+6。下列叙述正确的是
| A.X2-的离子半径大于Y+的离子半径 |
| B.H2Z的沸点高于H2X |
| C.Z的简单气态氢化物稳定性比W的强 |
| D.Y2X2和Y2Z的晶体类型和化学键类型完全相同 |
等质量的两份锌粉a和b,分别加入过量的稀硫酸中,并向a中加入少量CuSO4溶液,下图表示产生H2的体积(V)与时间(t)的关系,其中正确的是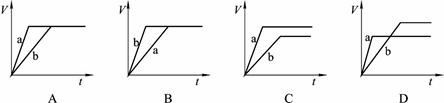
下列离子方程式正确的是
| A.把少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-= 2HClO+CaSO3↓ |
| B.足量铁屑溶于稀硫酸:2Fe+6H+=2Fe3++3H2↑ |
| C.碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O |
| D.铝片溶于烧碱溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
镭是元素周期表中第7周期第IIA族元素,下列有关叙述不正确的是
| A.镭的金属性比钙弱 | B.单质能与水反应生成H2 |
| C.镭在化合物中呈+2价 | D.碳酸镭难溶于水 |
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)
|
2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是
A.A、B、C的分子数之比为1∶3∶2X,Y,Z都是金属,在X与稀H2SO4反应中,加入少量Z的硫酸盐溶液时能使反应加快;X与Y组成原电池时,Y电极质量减少,X,Y,Z三种金属的活动性顺序为:
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |