某密闭容器中进行如下反应:X(g)+2Y(g)  2Z(g),要使平衡时反应物总物质的量与生成物的物质的量相等,且由X、Y作反应物,则X、Y的初始物质的量之比的范围应满足
2Z(g),要使平衡时反应物总物质的量与生成物的物质的量相等,且由X、Y作反应物,则X、Y的初始物质的量之比的范围应满足
A. < < < <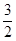 |
B. < < < < |
C.3< <4 <4 |
D.1< <3 <3 |
下列物质分解后不留残渣的是( )
| A.NaHCO3 | B.NH4HCO3 |
| C.KClO3 | D.CaCO3 |
下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是 ( )
A.SO2+H2O H2SO3 H2SO3 |
| B.Cl2+H2O=HCl+HClO |
C.3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2 |
| D.2Na+2H2O=2NaOH+H2↑ |
下列离子方程式书写正确的是 ( )
| A.碳酸钙与盐酸反应 CO32-+2H+=CO2↑+H2O |
| B.硫酸和氯化钡溶液反应 Ba2++SO42-=BaSO4↓ |
| C.氢氧化铜和硫酸反应 OH-+H+=H2O |
| D.铁钉放入硫酸铜溶液中 Fe+3Cu2+=2Fe3++3Cu |
下列化学反应基本类型中一定是氧化还原反应的是 ( )
| A.化合反应 | B.分解反应 |
| C.复分解反应 | D.置换反应 |
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是 ( )
| A.Na+、K+、OH-、Cl- |
| B.Na+、Cu2+、SO42-、NO3- |
| C.Mg2+、Na+、SO42-、Cl- |
| D.Ba2+、HCO3-、NO3-、K+ |