向某密闭容器中加入0.30mol A、0.10mol C和一定量的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图1所示.如图2为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各只改变一种条件,所改变的条件均不同.已知t3~t4阶段为使用催化剂.
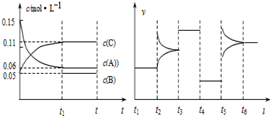
图1 图2
(1)若t1=20s,则t0~t1阶段以C浓度变化表示的反应速率为v(C)= ; t4~t5阶段改变的条件为 ;(t0为坐标原点)
(2)若t2~t3阶段,C的体积分数在不断地变小,则此阶段v(正) v(逆) (填“>”、“=”、“<”); t3~t4的平衡常数K= 。
(3)t5~t6阶段改变的条件为 ;B的起始物质的量为 ;
(4)t1达到平衡后,若保持容器温度和体积不变,再向容器中加入0.08mol A,0.2mol C,则平衡 (填“向正反应方向”、“向逆反应方向”或“不”)移动.
(5)在温度和容积不变条件下,能判断该反应达到平衡的依据是
A.混合气体的平均相对分子质量不变 B.反应体系的总压强不变
C.生成2mol C的同时生成3mol A D.2v生成(A)=3v生成(C)
下图是以C7H8为原料合成某聚酰胺类物质(C7H5NO)n的流程图.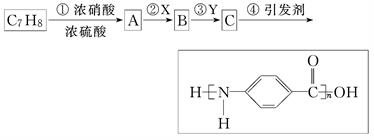
回答下列问题:
(1)聚酰胺类物质所具有的结构特征是________.(用结构简式表示)
(2)反应①通常应控制的温度为30℃左右,在实际生产过程中应给反应体系加热还是降温?为什么?____________________________________________________.若该反应在100℃条件下进行,则其化学反应方程式为_________________________________.
(3)反应②和反应③从氧化还原反应的角度看是________基团被氧化为________基团,________基团被还原为________基团.从反应的顺序看,应先发生氧化反应还是还原反应?为什么?_______________________________________________________________
_______________________.
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成,取m g该种氨基酸放在纯氧中充分燃烧.生成CO2、H2O和N2.现按下图装置进行实验,请完成下列问题:
(1)实验开始时,首先要通入一段时间的氧气,其理由是_____________________.
(2)以上装置中需要加热的仪器有________(填字母),操作时应先点燃________处的酒精灯.
(3)A装置中发生反应的化学方程式为_____________________________.
(4)装置D的作用是____________________________.
(5)读取N2的体积时,应注意①__________________,②________________________.
(6)实验中测得N2的体积为V mL(已折算成标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________.
| A.生成CO2气体的质量 | B.生成水的质量 |
| C.通入O2的体积 | D.氨基酸的相对分子质量 |
某有机物含有C、H、O、N四种元素,如图为该有机物的球棍模型.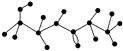
(1)该有机物的化学式________________,结构简式________________;
(2)该物质属于________;
A.有机物 B.氨基酸 C.二肽 D.糖 E.油脂
(3)该有机物可能发生的化学反应有(填编号)________;
①水解 ②加聚 ③取代 ④消去 ⑤酯化 ⑥与H2加成
(4)该有机物发生水解反应的化学方程式为______________________________.
在澄清的蛋白质溶液中加入以下几种物质:
(1)加入大量饱和食盐水,现象为________________,此过程叫做________.
(2)加入甲醛溶液,现象为________________,此过程称为蛋白质的________.
(3)加入浓硝酸并微热,现象为________________,这是由于浓硝酸与蛋白质发生了________反应的缘故.
(4)加热煮沸,现象为________________________________________________,
此过程称为蛋白质的________.
A、B、C、D都是只含有碳、氢、氧三种元素的有机物,在常温下A为气态,B、C为液态,D是白色晶体.A、B均有强烈的刺激性气味,C有果香味,D有甜味.它们具有相同的实验式,分别在足量氧气中充分燃烧后,恢复到室温下,其燃烧消耗O2的物质的量与燃烧产生的气体的物质的量相等.完成下列问题:
(1)上述有机物的实验式是________.
(2)写出下列物质的结构简式:A______________,B______________,C____________,D____________.