H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l) 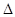 H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是
H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是
| A.电极a为电池的正极 |
B.电极b上发生的电极反应为:O2+2H2O+4e =" 4" OH =" 4" OH |
| C.电路中每流过4mol电子,电池内部释放632kJ热能 |
| D.每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
下列说法正确的是()
| A.1mol任何气体所占体积都约为22.4L |
| B.1molH2O在标准状况下体积为22.4L |
| C.1mol气体体积为22.4L,则一定是标准状况 |
| D.气体摩尔体积不一定是22.4L/mol |
下列物质中,含氢原子数目最多的是()
| A.0.9molH2O | B.0.3molH2SO4 | C.0.2molNH3 | D.0.4molCH4 |
标况下由0.5g H2、11g CO和4g O2组成的混合气体,其体积约为()
| A.8.4 L | B.11.2 L | C.14.0 L | D.16.8 L |
某原子的摩尔质量是Mg•mol﹣1,则一个该原子的真实质量约为()
| A.M g | B.1/M g | C.M/6.02×1023 g | D.6.02×1023/M g |
下列叙述中正确的是()
| A.1mol任何纯净物都含有相同的分子数 |
| B.1molO2中约含有6.02×1023个氧分子 |
| C.1mol氢中含有2mol氢原子 |
| D.阿伏加德罗常数就是6.02×1023mol﹣1 |