甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H1=" +" 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H2=-192.9 kJ·mol-1
下列说法正确的是
| A.CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) 的焓变△H = 3△H2 + 2△H1 |
B.应①中的能量变化如图所示 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ·mol-1 |
如图:A处通入氯气,关闭B阀时,C处湿润红色布条无变化,打开B阀时,C处湿润的红色布条褪色。则D中可以盛放足量的 ()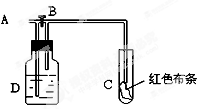
| A.浓硫酸 | B.氢氧化钠溶液 | C.水 | D.饱和食盐水 |
配制物质的量浓度为0.1mol•L-1的Na2CO3溶液100 mL时,下列操作正确的是
| A.用托盘天平称取1.06 g 无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中 |
| B.在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水 |
| C.定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分 |
| D.定容时,若仰视,则所配溶液的浓度将偏高 |
下列试剂的保存或使用正确的是()
| A.实验室的氯水需要保存在棕色试剂瓶中 |
| B.漂白粉比氯水稳定,可露置在空气中 |
| C.称量氢氧化钠固体时,可在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码 |
| D.金属钠可保存在煤油、四氯化碳等有机溶剂中 |
下列溶液中的氯离子浓度与50 mL 1 mol•L-1的AlCl3溶液中氯离子浓度相等的是
| A.150 mL 3 mol•L-1的KClO3溶液 |
| B.75 mL 2 mol•L-1的NH4Cl溶液 |
| C.150 mL 2 mol•L-1的CaCl2 溶液 |
| D.350 mL 3 mol•L-1的NaCl溶液 |
在同温同压下,A容器中的氧气(O2)和B容器中的氨气(NH3)所含的原子个数相同,则A、B两容器中气体的体积之比是()
A.1∶2 B.2∶1 C.2∶3 D.3∶2