室温下,将 0.1mol下列物质置于1L 水中充分搅拌后,溶液中阴离子数最多的是
| A.KC1 | B.MgCl2 | C.Na2CO3 | D.K2SO4 |
如图是某学校实验室从化学试剂商品店买回的硫酸试剂标签上的部分内容,据此,下列说法正确的是( )
| A.该硫酸的物质的量浓度为9.2 mol·L-1 |
| B.1 mol Zn与足量的该硫酸反应产生2 g氢气 |
| C.配制200 mL 4.6 mol·L-1的稀硫酸需取该硫酸50.0 mL |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol·L-1 |
下列表示对应化学反应的离子方程式正确的是()
| A.用氯化铁溶液腐蚀铜板:Cu+Fe3+=Cu2++Fe2+ |
B.Fe3O4与足量稀HNO3反应:3Fe3O4+28H++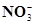 =9Fe3++NO↑+14H2O =9Fe3++NO↑+14H2O |
| C.用小苏打治疗胃酸过多:NaHCO3+H+=Na++CO2↑+H2O |
| D.往KAl(SO4)2溶液中滴入Ba(OH)2溶液至沉淀的物质的量最大: |
Al3+ + 2SO42- + 2Ba2+ + 4OH-="=" AlO2-+ 2BaSO4↓+ 2H2O
向下列物质的溶液中加入一定量的Na2O2固体,不出现浑浊现象的是( )
| A.饱和H2S溶液 | B.Ca(HCO3)2稀溶液 |
| C.K2SO3溶液 | D.FeCl2溶液 |
下列各组物质或概念之间,不符合右图所示关系的是()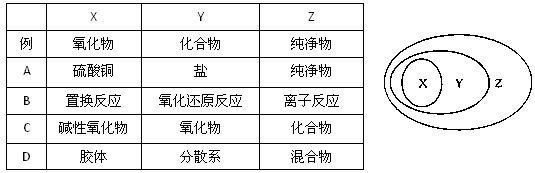
下列说法正确的是( )
①漂白粉、水玻璃和铝热剂都是混合物;
②煤的干馏和石油的分馏都是化学变化;
③氨基酸、纯碱、芒硝和生石灰分别属于酸、碱、盐和氧化物;
④乙醇中混有乙酸,除去乙酸可先加足量生石灰后再蒸馏。
| A.①③ | B.①④ | C.②④ | D.③④ |