某同学研究铝及其化合物的性质时设计了如下两个实验方案。
方案一:2.7g Al X溶液
X溶液 Al(OH)3沉淀
Al(OH)3沉淀
方案二:2.7g Al Y溶液
Y溶液 Al(OH)3沉淀
Al(OH)3沉淀
NaOH溶液和稀盐酸的浓度均是3 mol/L,如图二是向X溶液和Y溶液中分别加入NaOH溶液和稀盐酸时产生沉淀的物质量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是
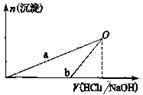
| A.X溶液溶质为AlCl3,Y溶液溶质为NaAlO2 |
| B.b曲线表示的是向X溶液中加入NaOH溶液 |
| C.在O点时两方案中所得溶液浓度相等 |
| D.a、b曲线表示的反应都是氧化还原反应 |
下列说法中正确的是( )
| A.在一定温度和压强下,各种气态物质体积大小由构成气体分子大小决定 |
| B.在一定温度和压强下,各种气态物质体积的大小由构成气体的分子数决定 |
| C.不同的气体,若体积不同,则它们所含的分子数一定不同 |
| D.气体摩尔体积是指1mol任何气体所占的体积约为22.4L |
下列分离或提纯物质的方法正确的是( )
| A.用蒸馏的方法制取蒸馏水 |
| B.用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D.用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质 |
下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液 ②PH试纸的使用 ③过滤 ④蒸发
| A.试管 | B.胶头 滴管 滴管 |
C.玻璃棒 | D.漏斗 |
进行化学实验必须注意安全。下列做法不正确的是()
| A.不慎将酒精灯打翻在桌上失火时,立即用湿抹布盖灭 |
| B.不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| C.配制浓硫酸时,可先在量筒中加一定体积水,再在搅拌下慢慢加入浓硫酸 |
| D.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 |
把物质的量均为0.1mol的AlCl3、CuCl2和H2SO4溶于水制成100ml的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同。则下列描述正确的是()
| A.电路中共转移0.9mol电子 |
| B.阳极得到的气体中有O2且其物质的量为0.35mol |
| C.阴极质量增加3.2g |
| D.铝元素以Al(OH)3的形式存在 |