由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、CO32-、Ba2+、SO42-。将该混合物溶于水后得澄清溶液,现取3份 100 mL该溶液分别进行如下实验:
| 实验序号 |
实验内容 |
实验结果 |
| 1 |
加入AgNO3溶液 |
有白色沉淀生成 |
| 2 |
加入足量NaOH溶液并加热 |
收集到气体1.12L(换算成标准状况) |
| 3 |
加入足量BaCl2溶液,,将所得沉淀洗涤、干燥、称重;再向沉淀中加足量的稀盐酸,洗涤、干燥、称重 |
第一次称重读数为6.27g,第二次称重读数为2.33g |
已知加热时NH4+ + OH-= NH3↑+ H2O, 试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是___________(填“一定存在”、“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是_________________。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度: 。
(3)试确定K+是否存在?__________(填“存在”或“不存在”),判断的理由是____________。
(4)若实验3中沉淀加稀盐酸后再洗涤,如何判断沉淀已洗净,方法是
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中Q所处的周期序数是其主族序数的一半,请回答下列问题:
⑴T的最高价氧化物对应的水化物为_____________。
⑵原子的得电子能力:Q______W(填“强于”或“弱于”)。
⑶原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________。
⑷W的单质与其最高价氧化物对应的水化物的浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_______________。
已知四种短周期元素形成的离子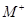 、
、 、
、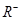 、
、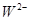 具有相同的电子层结构。(用推断出的元素符号表示)
具有相同的电子层结构。(用推断出的元素符号表示)
①M、N、R、W的原子序数由大到小的顺序是。
②M、N、R、W的原子半径由大到小的顺序是。
③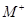 、
、 、
、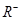 、
、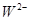 的离子半径由大到小的顺序是 。
的离子半径由大到小的顺序是 。
0.5mol 的Y元素的离子得到6.02×1023个电子被还原成中性原子,0.4gY的氧化物恰好与100ml 0.2mol .L-1 的盐酸完全反应,Y原子核内质子数和中子数相等。写出:
(1)Y的名称为,它在周期表的位置为
(2)Y的氧化物与盐酸反应的离子方程式为。
如图所示为短周期的一部分,如果B原子和C原子的核外电子总数之和为A的4倍,则B为(填元素符号)____________,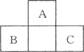
画出A的离子结构示意图: ______________,
C的最高价氧化物的分子式:__________________
用电子式表示A的氢化物分子的形成过程:
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: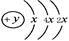 ,B、C可形成离子化合物B3C2,据此填空:
,B、C可形成离子化合物B3C2,据此填空:
(1)A的元素名称为,其气态氢化物的化学式为。
(2)A、B、C、D四种元素的原子,半径由小到大的顺序为。
(3)B和C最高价氧化物的水化物化学式分别为和。