已知1.505×1023个X气体分子的质量为16g,则X气体的摩尔质量是
| A.16g | B.32g | C.32g /mol | D.64g /mol |
下列物质属于非电解质的一组是
| A.盐酸、食盐、水银 | B.水玻璃、冰、火碱 |
| C.纯碱、铜绿、漂白粉 | D.干冰、液氨、酒精 |
下列仪器可以直接放在酒精灯火焰上加热的是
| A.烧杯 | B.蒸馏烧瓶 | C.蒸发皿 | D.量筒 |
下列叙述不正确的是
| A.根据一次能源和二次能源的划分,氢气为二次能源 |
| B.电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源 |
| C.火电是将燃料中的化学能直接转化为电能的过程 |
| D.在火力发电时,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化 |
参照反应Br+H2―→HBr+H的能量对反应历程的示意图,下列叙述中正确的是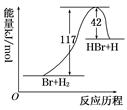
| A.正反应为吸热反应 |
| B.正反应为放热反应 |
| C.加入催化剂,该化学反应的反应热增大 |
| D.从图中可看出,该反应的反应热与反应途径有关 |
下列说法中正确的是
①只由一种元素组成的物质,一定是纯净物
②所有酸性氧化物都是非金属氧化物
③硝酸和氢硫酸均既有氧化性又有还原性
④化学反应的实质就是旧化学键断裂、新化学键形成的过程
| A.都正确 | B.①②④ | C.③④ | D.①② |