下图中“—”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙,下面四组选项中,符合图示要求的是()
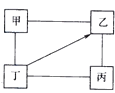
| |
甲 |
乙 |
丙 |
丁 |
| A. |
H2SO4 |
Na2SO4 |
NaOH |
NaCl |
| B. |
KCl |
K2CO3 |
KOH |
HCl |
| C. |
O2 |
CO2 |
CuO |
C |
| D. |
Fe |
CuCl2 |
Zn |
HCl |
A、B都是短周期元素,它们可形成化合物AB2,由此可以得出判断错误的是
A.A和B可能在同一周期 B.A和B可能在同一主族
C.A可能在第二周期ⅣA族 D.A肯定是金属元素
下列化学用语使用正确的是
A.硫原子的原子结构示意图: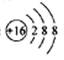 |
B.NH4Cl的电子式: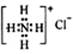 |
C.原子核内有10个中子的氧原子: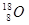 |
D.对氯甲苯的结构简式: |
下列各组物质中,所含化学键类型相同的是
| A.NaF、HNO3 | B.Na2O、H2O | C.HCl、MgCl2 | D.CO2、CH4 |
下列叙述正确的是
| A.配制0.1mol/L H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 |
| B.实验室制备Cl2,可用排饱和食盐水集气法收集 |
| C.实验室中,钠通常保存在盛有煤油的细口瓶中 |
| D.定容时仰视容量瓶刻度线,所配制的NaOH溶液浓度将偏高 |
下列有关物质性质的应用正确的是
| A.液氨汽化时要吸收大量的热,可用作制冷剂 |
| B.SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物 |
| C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D.氯化铝是一种电解质,可用于电解制铝 |