某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O ,3Cl2+6NaOH=5NaCl+ NaClO3 +3H2O),经测定ClO﹣与ClO3﹣的物质的量之比为1:2,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为] ( )
| A.21:5 | B.11:3 | C.3:1 | D.4:1 |
S2Cl2在合成橡胶、硬水软化等方面有着重要应用。将Cl2通入熔融的硫磺可制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊。有关叙述正确的是
| A.在周期表中,氯元素位于硫元素之后,所以Cl2的氧化性弱于硫单质 |
| B.Cl2与硫磺的反应中,S2Cl2只是氧化产物 |
| C.在常温常压下,硫磺是原子晶体,S2Cl2是分子晶体 |
| D.S2Cl2与水反应时,既体现氧化性又体现还原性 |
往含等物质的量的偏铝酸钠溶液与氢氧化钠的混合溶液中通入二氧化碳,产生沉淀的量与通入二氧化碳的量关系正确的是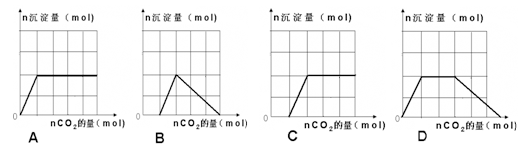
五种短周期元素的某些性质如表所示(其中只有W、Y、Z为同周期元素)。
| 元素代号 |
X |
W |
Y |
Z |
Q |
| 原子半径(×10-12 m) |
37 |
64 |
66 |
70 |
154 |
| 主要化合价 |
+1 |
-1 |
-2 |
+5、-3 |
+1 |
下列说法正确的是
A.由Q与Y形成的化合物中只存在离子键
B.Z与X之间形成的化合物具有还原性
C.由X、Y、Z三种元素形成的化合物,其晶体一定是分子晶体
D.Y与W形成的化合物中,Y显负价
X、Y、Z、W有如图所示的转化关系,则X、Y可能是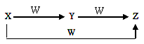
①C、CO ②S、SO2③AlCl3、Al(OH)3 ④Cl2、FeCl3
A.仅有①③ B.①②③ C.仅有②④ D.①②③④
下列离子反应方程式正确的是
A.铜粉与98.3%的硫酸加热下反应:Cu + 4H+ + SO42― Cu2++ SO2↑+ 2H2O Cu2++ SO2↑+ 2H2O |
B.电解饱和食盐水:2Cl- +2H+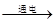 H2↑+C12↑ H2↑+C12↑ |
| C.向氯化铝溶液中加入过量氨水:Al3++ 4NH3·H2O=[Al(OH)4]-+ 4NH4+ |
| D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |