以下实验操作简便、科学且成功的是( )
| A.将乙酸和乙醇的混合物注入浓硫酸中制备乙酸乙酯 |
| B.将铜丝在酒精灯的外焰上加热变黑后,插入乙醇溶液中铜丝又恢复到原来的红色 |
| C.往试管中注入2mLCuSO4溶液,再滴几滴NaOH溶液后,加入乙醛溶液即有红色沉淀产生 |
| D.向淀粉溶液中加入稀硫酸加热,一段时间后,再加入银氨溶液检验是否水解 |
用标准电极电解NaCl和CuSO4的25 0ml混合溶液,经过一段时间后,两极分别得到11.2L(标准状况下)的气体。则原溶液中NaCl的物质的量浓度不可能是()
0ml混合溶液,经过一段时间后,两极分别得到11.2L(标准状况下)的气体。则原溶液中NaCl的物质的量浓度不可能是()
| A.0.5mol/L | B.1mol/L | C.1.5mol/L | D.4mol/L |
反应2X(g)+Y(g) 2Z(g)△H﹤0,在不同温度(T1和T2
2Z(g)△H﹤0,在不同温度(T1和T2 )及压强(p1和p2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下述判断正确的是
)及压强(p1和p2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下述判断正确的是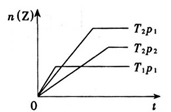
A.T1<T2,p1<p2 |
B.T1<T2,p1>p2 |
| C.T1>T2,p1>p2 | D.T1>T2,p1<p2 |
100ml 浓度为2mol/L的盐酸跟过量的锌 片反应,为加快反应速率,又不影响生成氢气总量,可采用的方法是
片反应,为加快反应速率,又不影响生成氢气总量,可采用的方法是
| A.加入少量浓盐酸 | B.加入几滴氯化铜溶液 |
| C.加入适量蒸馏水 | D.加入适量的氯化钠溶液 |
2SO2+O2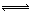 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
合成氨工业上,采用循环利用操作的主要目的是
| A.加快反应速率 | B.提高氨气的平衡浓度 |
| C.降低氨气的沸点 | D.提高N2和H2的利用率 |