下列表示对应化学反应的离子方程式正确的是
| A.氢氧化亚铁在空气中的变化:4Fe(OH)2 + 2H2O +O2= 4Fe(OH)3 |
| B.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O =AlO2-+4NH4++2H2O |
| C.向Ca(HCO3)2溶液中滴加过量的NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D.用FeCl3溶液腐蚀铜线路板:Cu + Fe3+= Cu2+ + Fe2+ |
纯净物X、Y、Z转化关系如下图所示,下列判断正确的是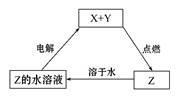
| A.Z可能是氯化钠 | B.Z可能是三氧化硫 |
| C.X可能是金属铜 | D.Y不可能是氢气 |
下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:2的有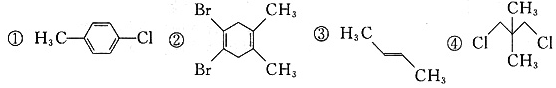
| A.0种 | B.1种 | C.2种 | D.3种 |
下列实验中,所采取的分离方法与对应原理都正确的是
| 选项 |
目的 |
分离方法 |
原理 |
| A. |
除去丁醇中的乙醚 |
蒸馏 |
丁醇与乙醚的沸点相差较大 |
| B. |
分离乙酸乙酯和乙醇 |
分液 |
乙酸乙酯和乙醇的密度不同 |
| C. |
除去KNO3固体中混杂的NaCl |
重结晶 |
NaCl在水中的溶解度很大 |
| D. |
分离溶于水的碘 |
乙醇萃取 |
碘在乙醇中的溶解度较大 |
25℃时,将a mol·L-1一元酸HA与b mol·L-1 NaOH等体积混合后测得溶液pH=7,则下列关系一定不正确的是
| A.a=b | B.a>b | C.c(A-)=c(Na+) | D.c(A-)<c(Na+) |
化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:
NH3+H2O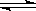 NH3·H2O
NH3·H2O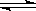 NH4++OH-
NH4++OH-
(1)向氨水中加入MgCl2固体时,平衡向______反应方向移动,现象为____________。
(2)向氨水中通入HCl,平衡向_______反应方向移动,此时溶液中浓度减小的粒子有___________、___________、___________。
(3)向浓氨水中加入少量碱石灰,平衡向______反应方向移动,溶液pH值_________(填“增大”、“减小”或“不变”),现象为______________________。实验室常利用该原理制备氨气,在此过程中碱石灰的另一个作用是_______。