在无色、碱性溶液中能大量共存的一组离子是
| A.Ca2+、Na+、SO42﹣、HCO3﹣ |
| B.K+、Fe2+、SO42﹣、MnO4﹣ |
| C.Ba2+、K+、Al3+、Cl﹣ |
| D.Na+、Ba2+、Cl﹣、NO3﹣ |
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
| 实验 |
反应温度/℃ |
Na2S2O3溶液 |
稀H2SO4 |
H2O |
||
| V/ml |
c/(mol·L—1) |
V/ml |
c/(mol·L—1) |
V/mL |
||
| A |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
| B |
25 |
5 |
0.2 |
5 |
0.2 |
10 |
| C |
35 |
5 |
0.1 |
10 |
0.1 |
5 |
| D |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
据报道,在300 ℃、70 MPa条件下由二氧化碳与氢气合成乙醇已成为现实2CO2(g)+6H2(g)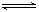 CH3CH2OH(g)+3H2O(g)。下列叙述错误的是( )
CH3CH2OH(g)+3H2O(g)。下列叙述错误的是( )
| A.使用Cu-Zn-Fe催化剂可大大提高生产效率 |
| B.反应需在300 ℃进行,可推测该反应是吸热反应 |
| C.充入大量CO2气体可提高H2的转化率 |
| D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率 |
在恒温、体积为2 L的密闭容器中进行反应:2A(g)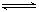 3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为( )
3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为( )
A.v(B)=0.03 mol·L-1·s-1
B.v(B)=0.045 mol·L-1·s-1
C.v(C)=0.03 mol·L-1·s-1
D.v(C)=0.06 mol·L-1·s-1
一定温度下在一容积恒定的密闭容器中,进行如下可逆反应:2A(g)+B(s)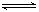 C(g)+D(g)。当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
C(g)+D(g)。当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
①容器内混合气体的密度②容器内混合气体的压强③容器内混合气体的总物质的量④容器内C物质的物质的量浓度
| A.①④ | B.②③ |
| C.②③④ | D.④ |
对于可逆反应:2SO2(g)+O2(g)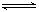 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
| A.增大压强 | B.升高温度 |
| C.使用催化剂 | D.多充O2 |