事实上,许多非金属氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2 +SO2 = Na2SO4 2Na2O2 +2SO3= 2Na2SO4 +O2据此,你认为下列反应方程式中正确的是
| A.2Na2O2 + 2N2O4= 4NaNO3 |
| B.Na2O2 + 2NO2 = 2NaNO2 + O2 |
| C.2Na2O2 + 2N2O3= 4NaNO2 + O2 |
| D.2Na2O2 + 2 Mn2O7 = 4Na2MnO4 + O2 |
常温下,下列各组离子在指定溶液中,一定能大量共存的是
| A.在0.1 mol·L-1NaOH溶液中:K+、Na+、SO42-、HCO3- |
| B.在0.1 mol·L-1Na2CO3溶液中:A13+、Na+、NO3-、C1- |
| C.在0.1 mol·L-1FeCl3溶液中:K+、NH4+、I-、SCN- |
| D.在c(H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3- |
乳酸的结构简式为  ,下列有关乳酸的说法中,不正确的是
,下列有关乳酸的说法中,不正确的是
| A.乳酸中能发生酯化反应的官能团有2种 |
| B.1 mol乳酸可与2 mol NaOH发生中和反应 |
| C.1 mol乳酸与足量金属Na反应生成1 mol H2 |
D.有机物  与乳酸互为同分异构体 与乳酸互为同分异构体 |
下列实验操作中,能达到相应实验目的的是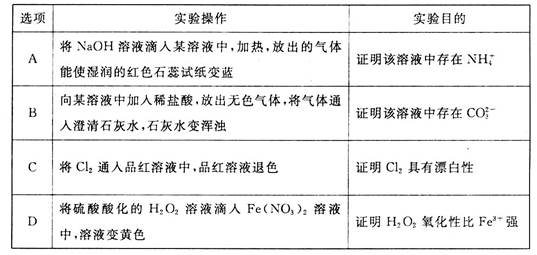
下列物质分别与水溶液中的Fe3+发生反应,并生成等量的Fe2+时,消耗还原剂的物质的量最少的是
| A.Cu | B.Fe | C.SO2 | D.I- |
W、X、Y、Z是四种短周期元素,其原子序数依次增大。已知甲是由其中三种元素组成的化合物,25℃时0.1 mo1.L-1甲溶液的pH为13。X元素的气态氢化物可与其最高价氧化物对应的水化物反应生成盐。下列说法中,正确的是
| A.原子半径大小的比较:r(X)>r(Y)>r(Z) |
| B.元素Y、Z的简单离子的电子层结构不同 |
| C.元素X的简单气态氢化物的热稳定性比元素Y的强 |
| D.只含W、X、Y三种元素的化合物中,有离子化合物,也有共价化合物 |