下列有关说法错误的是
| A.H2O2、Na2O2都属于过氧化物、都存在非极性共价键 |
| B.H2O2做漂白剂是利用其强氧化性,漂白原理与HClO类似但与SO2不同 |
| C.双氧水是绿色氧化剂,可作医疗消毒剂 |
| D.H2O2既有氧化性又有还原性,1molH2O2在参加反应时一定转移2mol电子 |
下列说法中正确的是()
| A.煤的气化是化学变化,煤的液化是物理变化 |
| B.甲烷是一种清洁燃料,可用作燃料电池的燃料 |
| C.蔗糖与淀粉水解的最终产物都是葡萄糖 |
| D.石油分馏可以得到乙烯、丙烯、甲烷等化工原料 |
“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学概念的是()
| A.乙烯聚合为聚乙烯高分子材料 | B.甲烷与氯气制备一氯甲烷 |
| C.以铜和浓硝酸为原料生产硝酸铜 | D.用二氧化硅制备高纯硅 |
化学与我们的生活、社会密切相关,下列说法不正确的是()
| A.蛋白质遇浓硝酸变黄是发生了颜色反应 |
| B.富含蛋白质的食物多属于酸性食物,蔬菜、水果多属于碱性食物 |
| C.麻黄碱是一种天然药物,能增加人的兴奋程度,运动员可以使用 |
| D.碘元素是人体神经系统发育所不可缺少的“智力元素” |
为测定某镁铝合金样品中铝的含量,进行下列实验:取一定量合金,加入100mL0.3mol·L-1稀硫酸,合金完全溶解,产生的气体在标况下为.560mL;再加入0.2mol·L-1NaOH溶液至沉淀质量不再变化,用去350mLNaOH溶液。则所取样品中铝的物质的量为
| A.0.005 mol | B.0.01mol | C.0.025mol | D.0.03 mol |
某温度下,将等物质的量的A、B、C、D四种物质混合于一恒容密闭容器中,发生如下反应:aA(g)+bB(g)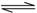 cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是()
cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是()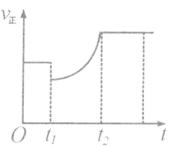
A.达到化学平衡时A的消耗速率与C的消耗速率相等
B.保持温度不变,再向容器中充人llmolA和n/2molB,平衡不移动
C.上图表示该反应的正反应速 率随时间的变化情况,t1时刻可能是减少了A的浓度,增加了C的浓度
率随时间的变化情况,t1时刻可能是减少了A的浓度,增加了C的浓度
D.保持温度不变,再向容器中充人nmolA和nmolB,A、B的转化率均不变