下列说法中,正确的是
| A.反应产物的总能量大于反应物的总能量时,△H< 0 |
B.已知反应H2 (g)+I2(g) 2HI(g)平衡常数为K,则2H2 (g)+2I2(g) 2HI(g)平衡常数为K,则2H2 (g)+2I2(g) 4HI(g)的平衡常数为2K 4HI(g)的平衡常数为2K |
| C.ΔH<0、ΔS>0的反应在温度低时不能自发进行 |
| D.在其他外界条件不变的情况下,使用催化剂,不能改变化学反应进行的方向 |
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42﹣、NO3﹣、Cl﹣中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法不正确的是
| A.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| C.该溶液中所含的离子是:Fe2+、Na+、SO42﹣、NO3﹣ |
| D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
下列有关说法正确的是
| A.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀。 |
B.2NO(g)+2CO(g) N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0。 N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0。 |
| C.加热0.1 mol·L-1 Na2CO3溶液,CO32-水解程度和溶液的pH均增大。 |
| D.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大。 |
一定条件下,通过下列反应可实现燃煤烟气中硫的回收,其中Y是单质。
SO2(g) + 2CO(g) 2X(g)+Y(l)
2X(g)+Y(l)
为了测定在某种催化剂作用下的反应速率,在某温度下用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表: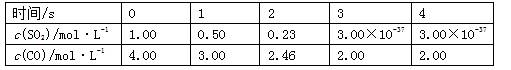
下列说法不正确的是
| A.X的化学式为CO2 |
| B.前1s内v(X)= 1.00 mol·L-1·s-1 |
| C.该回收原理运用了SO2的还原性 |
| D.该温度下,此反应的平衡常数的数值是3.33×1036 |
将足量的CO2通入下列各溶液中,所含离子还能大量共存的是
| A.K+、SiO32-、Cl-、NO3- | B.H+、NH4+、Al3+、SO42- |
| C.Na+、S2-、OH-、SO42- | D.Na+、C6H5O-、CH3COO-、HCO3- |
下列说法不正确的是
| A.甲苯和环己烯都能使酸性高锰酸钾溶液褪色 |
| B.用银氨溶液可以鉴别乙醛和葡萄糖溶液 |
| C.甲醛和乙二醇都可作为合成高分子化合物的单体 |
| D.丙烷和2-甲基丙烷的一氯代物均为两种 |