将4 mol SO2与2 mol O2放入4L的密闭容器中,在一定条件下反应:2SO2(g)+O2(g) 2SO3(g),测得平衡时SO3的浓度为0.5 mol·L-1。则此条件下的平衡常数K(单位为L·mol-1)为
2SO3(g),测得平衡时SO3的浓度为0.5 mol·L-1。则此条件下的平衡常数K(单位为L·mol-1)为
| A.4 | B.0.25 | C.0.4 | D.0.2 |
关于下列实验装置或操作的说法中,正确的是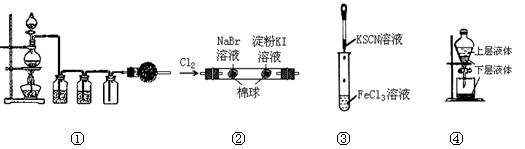
| A.①可用于实验室用MnO2固体与浓盐酸共热制取Cl2,并进行干燥、除杂 |
| B.②实验中若左边棉花变黄色,右边棉花变蓝色,则能证明氧化性:Cl2>Br2>I2 |
| C.③实验试管中会生成血红色沉淀 |
| D.④装置用来提取碘的四氯化碳溶液中的碘单质 |
在一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可以看到灰黑色粉末,其中有些已变成棕褐色。将上述粉末溶于稀盐酸,取上层清液,滴入几滴氯水,再滴加KSCN溶液,马上出现血红色。以下结论不正确的是
| A.该灰黑色粉末用作抗氧化剂 |
| B.该灰黑色粉末不可食用 |
| C.粉末变为棕褐色是因为与空气中的氧气作用 |
| D.该灰黑色粉末在起作用的过程中作为氧化剂 |
下列四种有色溶液与SO2气体作用均能褪色,其反应实质相同的是
①酸性高锰酸钾溶液;②品红溶液;③溴水;④滴有酚酞的氢氧化钠溶液
| A.①③ | B.②③ | C.①④ | D.②④ |
在强酸性溶液中能大量共存的无色透明离子组是
| A.K+、Na+、CH3COO-、Cl- | B.Mg2+、Na+、Cl-、SO42- |
| C.MnO4—、Na十、SO3-、Br- | D.Na十、Ba2+、OH-、SiO32- |
NA表示阿伏加德罗常数,下列说法正确的是
| A.常温下,32g O2与32g O3所含的氧原子数均为2NA |
| B.2.4g金属镁变为镁离子时失去的电子数为0.1NA |
| C.1.0 L 1.0 mol·L-1 CH3COOH溶液中含有的CH3COO—数目为NA |
| D.14g14C中所含有的中子数为6NA |