能正确表示下列反应的离子方程式为
| A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C.NaClO和NaOH的混合溶液中通入少量的SO2:ClO-+H2O+SO2=C1-+SO42- +2H+ |
| D.大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
现有四种元素的基态原子的电子排布式如下①1s22s22p63s23p4 ②1s22s22p63s23p3; ③1s22s22p5下列正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③>②>① | D.不成对电子数:③>②>① |
4p轨道电子排布达到半充满的元素,其原子序数是
| A.15 | B.33 | C.35 | D.51 |
气态中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是
| A.1s22s22p63s23p2→1s22s22p63s23p1 |
| B.1s22s22p63s23p3→1s22s22p63s23p2 |
| C.1s22s22p63s23p4→1s22s22p63s23p3 |
| D.1s22s22p63s23p63d104s24p1 →1s22s22p63s23p63d104s2 |
基态原子的价电子构型3s23p3,下列关于它的描述正确的是
| A.该元素的电负性小于1.8 |
| B.3p能级上的3个电子能量相等,自旋状态相同 |
| C.它的氢化物分子中有四个键合电子 |
| D.该元素的价电子数是4 |
基态硅原子的电子排布图正确的是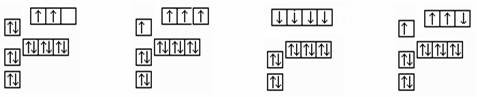
A B C D