肼(N2H2 )是火箭常用的高能燃料,常温下为液体,其球棍模型如下图所示。肼能与双氧水发生反应: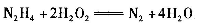 。用NA表示阿伏伽德罗常数,下列说法正确的是
。用NA表示阿伏伽德罗常数,下列说法正确的是
| A.标准状况下,11.2LN2 中含电子总数为5 NA |
| B.标准状况下,22.4LN2 H4中所含原子总数为6 NA |
| C.标准状况下, 3.2gN 2H4中含有共价键的总数为0.6 NA |
| D.若生成3.6gH2 O,则上述反应转移电子的数目为0.2 NA |
右图是一种常见有机物的比例模型,该模型图可代表一种
| A.饱和一元醇 | B.饱和一元醛 |
| C.羧酸酯 | D.羟基酸 |
下列关于有机物的说法正确的是
| A.将甲烷通入溴水中能发生取代反应 |
| B.乙烯双键中的一个键可以断裂,容易发生加成反应 |
| C.乙酸是一种重要的有机酸,是一种无色无味的液体 |
| D.由于乙醇的密度比水小,所以乙醇溶液中的水可以通过分液的方法除去 |
下列根据实验现象所得出的结论中,一定正确的是( )
| A.无色溶液使红色石蕊试纸变蓝,结论:溶液显碱性 |
| B.无色溶液焰色反应呈黄色,结论:溶液是钠盐溶液 |
| C.无色溶液加入Na2CO3溶液产生白色沉淀,结论:溶液中含Ca(OH)2 |
| D.某气体能使红色石蕊试纸变蓝,结论:该气体为NH3 |
已知铍(Be)的原子序数为4,下列对铍及其化合物的叙述中,正确的是 ( )
| A.铍的原子半径大于硼的原子半径 |
| B.氯化铍分子中铍原子的最外层电子数是8 |
| C.氢氧化铍的碱性比氢氧化钙的弱 |
| D.单质铍跟冷水反应产生氢气 |
下列叙述正确的是 ()
| A.同主族金属的原子半径越大熔点越高 |
| B.稀有气体原子序数越大沸点越高 |
| C.分子间作用力越弱分子晶体的熔点越低 |
| D.同周期元素的原子半径越小越易失去电子 |