下列说法中正确的是
| A.干冰升华时分子内共价键会发生断裂 |
| B.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
| C.分子晶体的熔沸点低,常温下均呈液态或气态 |
| D.金属导电的原因是在外加电场的作用下金属产生自由电子,电子定向运动 |
下列仪器常用于物质分离的是()
| A.①③⑤ | B.②③⑤ | C.②④⑤ | D.①②⑥ |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( ) 



A B C D
m g H2O2与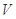 L(标准状况)CO中所含氧原子数目相同,则m的数值是( )
L(标准状况)CO中所含氧原子数目相同,则m的数值是( )
A.17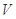 /22.4 /22.4 |
B.28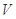 /22.4 /22.4 |
C.34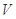 /22.4 /22.4 |
D.14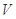 /22.4 /22.4 |
在标准状况下,将wg A气体(摩尔质量为Mg/mol)溶于1L水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度为( )mol/L
A.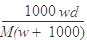 |
B.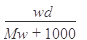 |
C.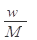 |
D.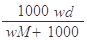 |
下列现象或应用中,不涉及胶体性质的是( )
| A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
| B.清晨,在茂密的树林中,常可以看到从枝叶间透过的光柱 |
| C.用半透膜分离淀粉和食盐的混合液 |
| D.肾功能衰竭等疾病引起的血液中毒,可用血液透析进行治疗 |