设NA为阿伏伽德罗常数,下列叙述正确的是
| A.常温常压下,28 g C2H4和CO的混合气体中含有碳原子的数目为1.5NA |
| B.1L0.1mol·L-1乙酸溶液中H+数为0.1NA |
| C.1mol甲烷分子所含碳氢键数为4NA |
| D.标准状况下,22.4L乙醇的分子数为NA |
已知丙酮(C3H6O)通常是无色液体,易溶于水,密度小于1 g·mL-1,沸点约为55℃。要从水与丙酮的混合物中将丙酮分离出来,下列方法中最为合理的是
| A.分液 | B.蒸馏 | C.过滤 | D.蒸发 |
以下实验装置一般不用于分离物质的是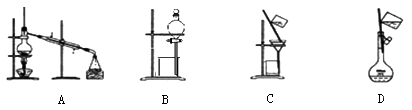
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入
| A.0.15 mol CuO | B.0.05 mol Cu2(OH)2CO3 |
| C.0.075mol Cu(OH)2 | D.0.1 mol CuCO3 |
在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法正确的是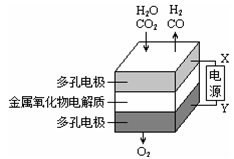
| A.X是电源的正极 |
| B.阴极的反应式是:H2O+2eˉ=H2+O2ˉ、CO2+2eˉ=CO+O2ˉ |
C.总反应可表示为:H2O+CO2 H2+CO H2+CO |
| D.阴、阳两极生成的气体的物质的量之比是1︰1 |
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是
| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |