NA代表阿伏加德罗常数,下列叙述错误的是
| A.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% |
| B.在H2O2+Cl2===2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 |
| C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| D.一定温度下,1 L 0.50 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1 NH4Cl的溶液含NH的物质的量不同 |
根据下列实验内容得出的结论正确的是
| 实验操作 |
解释或结论 |
|
| A |
 沉淀中滴入浓KCI溶液有白色沉淀出现 沉淀中滴入浓KCI溶液有白色沉淀出现 |
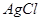 比 比 更难溶 更难溶 |
| B |
某物质的水溶液能使红色石蕊试纸变蓝 |
该物质一定是氨气 |
| C |
滴加氯水和 振荡,静置,下层溶液为紫色 振荡,静置,下层溶液为紫色 |
原溶液中有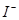 |
| D |
用洁净的铂丝蘸取溶液进行焰色反应,火焰呈黄色 |
含有Na单质 |
下列有关离子方程式或热化学方程式书写正确的是
A.石灰乳与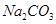 溶液混合: 溶液混合: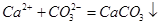 |
B.用惰性电极电解氯化镁溶液: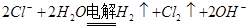 |
C.将碳与足量的浓硫酸共热反应后的气体混合物,通入过量氢氧化钠溶液中: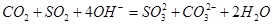 |
D.84消毒液和洁厕灵混合使用会产生有毒气体: |
短周期元素W、X、Y和Z的原子序数依次增大,金属W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法正确的是
A.由金属W制备的高效电池可用 溶液作电解质 溶液作电解质 |
| B.元素Y、Z的最高价氧化物对应水化物之间可以发生反应 |
| C.元素X、Z形成的化合物为离子化合物 |
D.四种元素原子半径由大到小的顺序为: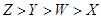 |
用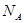 表示阿伏加德罗常数的值。下列叙述中不正确的是
表示阿伏加德罗常数的值。下列叙述中不正确的是
A.足量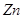 与一定量的浓硫酸反应,产生 与一定量的浓硫酸反应,产生 (标况)气体时,转移的电子数为 (标况)气体时,转移的电子数为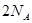 |
B.一定条件下,32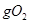 和足量的铁粉充分反应,转移的电子数为 和足量的铁粉充分反应,转移的电子数为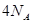 |
C.4.6g乙醇和甲酸(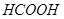 )的混合物中含有的碳原子数在 )的混合物中含有的碳原子数在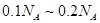 之间 之间 |
D.分子总数为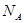 的NO和 的NO和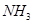 混合气体中含有的氮原子数为 混合气体中含有的氮原子数为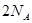 |
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
| a |
b |
c |
|
| A |
 |
 |
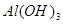 |
| B |
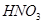 |
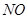 |
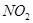 |
| C |
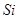 |
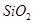 |
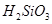 |
| D |
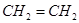 |
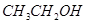 |
 |