可以大量共存的离子组是
| A.Na+、Fe2+、NO3-、Cl- |
| B.K+、HCO3-、SO42-、OH- |
| C.ClO-、Cl-、Na+、H+ |
| D.Ba2+、K+、SO42-、H+ |
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是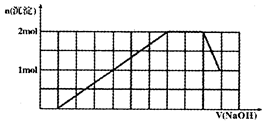
| A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+ |
| B.原溶液中一定含有SO42-和Na+ |
| C.原溶液中SO42-的物质的量至少为4.5mol |
| D.反应最后形成的溶液中含有的溶质为Na2SO4 |
下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、N两种元素的气态氢化物的稳定性相比,前者较弱 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
下列离子方程式书写正确的是
A.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2 +6H++5H2O2=2Mn2++5O2↑+8H2O +6H++5H2O2=2Mn2++5O2↑+8H2O |
B.将少量SO2通入苯酚钠溶液中:2C6H5O-+SO2+H2O=2C6H5OH+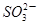 |
| C.用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-=Fe(SCN)3↓ |
| D.向碘化亚铁溶液中通入过量的氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
有机物X、Y、M(M为乙酸)的转化关系为:淀粉→X→Y 乙酸乙酯,下列说法错误的是
乙酸乙酯,下列说法错误的是
| A.X可用新制的氢氧化铜检验 |
| B.由Y和M制取乙酸乙酯时可用饱和NaOH溶液来提纯 |
| C.由Y生成乙酸乙酯的反应属于取代反应 |
| D.可用碘的四氯化碳溶液检验淀粉是否水解完全 |
下列对于生产、生活有关的化学问题的分析正确的是
| A.对“地沟油”进行分馏可得到汽油 |
| B.向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 |
| C.PM 2.5、二氧化碳都属于空气质量日报的内容 |
| D.误食可溶性重金属盐后,应采取的有效应急措施是喝大量的豆浆或牛奶 |