SO2是一种大气污染物,可用NaOH溶液除去,下列有关解释的方程式不合理的是
| A.SO2在大气中能最终生成H2SO4:2SO2+O2+2H2O=4H++2SO42- |
| B.少量SO2与NaOH溶液反应的离子方程式是:SO2+OH-=HSO3- |
| C.NaOH溶液缓慢吸收过量SO2的过程中有:SO2+SO32-+H2O=2HSO3- |
D.n(SO2): n(NaOH)=1:2时,溶液pH>7:SO32-+H2O  HSO3-+ OH- HSO3-+ OH- |
已知NA代表阿伏加德罗常数,下列说法正确的是
| A.34 g H2O2中含有的阴离子数为NA |
| B.标准状况下,22.4 L O2 作氧化剂时转移电子数一定为4NA |
C.T ℃时,1 L pH=6纯水中,含10-6NA个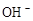 |
| D.10 L 0.1 mol·L-1的Na2CO3溶液中,Na+、CO32-总数为3 NA |
某无色溶液中滴入石蕊试液显红色,该溶液中可以大量共存的是
| A.Na+、Cl-、Mg2+、ClO- | B.Fe2+、NH4+、Cl-、NO3一 |
| C.Na+、HCO3-、AlO2一、K+ | D.Na+、Ba2+、Cl-、NO3一 |
下列说法正确的是
| A.金属氧化物均不能与氢氧化钠溶液反应 |
| B.BaCO3饱和溶液几乎不导电,所以BaCO3是非电解质 |
| C.点燃的镁条在N2中不能继续燃烧 |
| D.一定条件下,在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓 |
下列有机物命名正确的是
| A.3,3-二甲基丁烷 | B.2-乙基-1-戊烯 | C.4-甲基-3-乙基庚烷 | D.2-甲基-3-戊烯 |
下列物质中没有顺反异构的是
| A.1,1-二氯乙烯 | B.1,2-二氯丙烯 | C.2-甲基-2-丁烯 | D.1-氯-1-丙烯 |