氨气是重要化工产品之一。传统的工业合成氨技术的反应原理是:N2(g)+3H2(g) NH3(g)ΔH=-92.4 kJ/mol。在500 ℃、20 MPa时,将N2、H2置于一个固定容积的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题:
NH3(g)ΔH=-92.4 kJ/mol。在500 ℃、20 MPa时,将N2、H2置于一个固定容积的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题:

(1)计算反应在第一次平衡时的平衡常数K= 。(保留二位小数)
(2)产物NH3在5~10 min、25~30min和45~50 min时平均反应速率(平均反应速率分别以v1、v2、v3表示)从大到小排列次序为 。
(3)H2在三次平衡阶段的平衡转化率分别以α1、α2、α3表示,其中最小的是 。
(4)由第一次平衡到第二次平衡,平衡移动的方向是_______,采取的措施是________。
(5)请在下图中用实线表示25~60min 各阶段化学平衡常数K的变化图像。

【化学-有机化学基础】
北京市疾病预防控制中心的调查结果显示,在北京市场上有九成受检香水和三成护发类化妆品被查出致癌物”邻苯二甲酸酯”(PAEs),值得注意的是,在儿童护肤类化妆品中亦有两件样品分别被检出邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二(2-乙基己基)(DEHP)。
(1)邻苯二甲酸二乙酯(DEP)的结构简式为,其核磁共振氢谱共有组吸收峰,峰面积之比为。
(2)以下是某课题组设计的合成邻苯二甲酸二乙酯(DEP)的路线: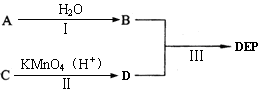
已知:

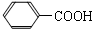
①C的结构简式为,其一溴代物有种。
②反应Ⅰ属于反应,反应Ⅲ属于反应。
③D和乙二醇在一定条件下可以发生反应生成一种高分子化合物,写出化学方程式。
纳米TiO2具有独特的光催化性、优异的颜色效应以及紫外线屏蔽等功能,在光催化剂、化妆品、抗紫外线吸收剂、功能陶瓷、气敏传感器件等方面具有广阔的应用前景。工业上用钛铁精矿(FeTiO3)提炼TiO2的工艺流程如下: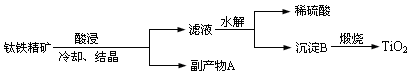
(1)写出硫酸酸浸溶解钛铁精矿的离子方程式,酸浸时为了提高浸出率,可以采取的措施为。
(2)钛铁精矿后冷却、结晶得到的副产物A为,结晶析出A时,为保持较高的酸度不能加水,其原因可能为 。
(3)滤液水解时往往需加大量水稀释同时加热,其目的是。
(4)上述工艺流程中体现绿色化学理念的是。
(5)工业上将TiO2和炭粉混合加热氯化生成的TiCl4,然后在高温下用金属镁还原TiCl4得到金属钛,写出TiO2制备Ti的化学方程式:。
浸出-萃取-电积法已成为铜湿法冶金的主要工艺过程。以黄铜铜为原料,采用电积法生产阴极铜生产线,主要生产工艺为:
黄铜铜→硫酸浸出→过滤→萃取→反萃→电积→阴极铜。
(1)浸出是用浸矿剂将铜矿石中的铜进入溶液中。据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下,酸性溶液中,将黄铜矿氧化成硫酸盐,写出用硫酸浸出黄铜矿发生反应的离子方程式:。
(2)萃取是利用特效铜萃取剂在含铜、铁及其碱性金属离子的低浓度含杂浸出液中有选择性地使铜离子萃入有机相,将铜离子与其它金属离子有效地分离,并通过反萃取使低浓度铜离子的原液富集成适宜电积要求的硫酸铜溶液。萃取过程的化学平衡为:2RH+Cu2+ R2Cu+2H+。则萃取和反萃取进行的程度受和的影响。
R2Cu+2H+。则萃取和反萃取进行的程度受和的影响。
(3)电积是将萃取富集后的铜溶液电解沉积出阴极铜。右图为用惰性阳极电积阴极铜的装置图:
①在图示方框中标出电源的正负极。
②写出电积阴极铜的总反应。
(4)金属铜长期露置于空气中容易生锈,铜锈的主要成分为,请利用电化学原理画出防止铜腐蚀的装置图。
(1)I.短周期某主族元素M的电离能情况如右图(A)所示。则M元素位于周期表的第族。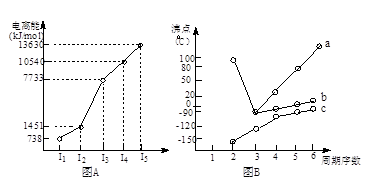
II.图B折线c可以表达出第族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:__________(填“a”或“b”)
III.部分有机物的熔沸点见下表:
| 烃 |
CH4 |
CH3CH3 |
CH3(CH2)2CH3 |
硝基苯酚 |
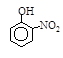 |
 |
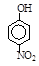 |
| 沸点/℃ |
-164 |
-88.6 |
-0.5 |
熔点/℃ |
45 |
96 |
114 |
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):
,
。
(2)COCl2俗称光气,分子中C原子采取杂化成键;其中碳氧原子之间共价键含有
________(填字母):
a.2个σ键;b.2个π键;c.1个σ键.1个π键。
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种晶体的样品配成溶液;b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的2/3。则绿色晶体配合物的化学式为。
(16分) 氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300-1700oC的氮气流中反应制得3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)上述反应氧化剂是,已知该反应每转移1mole—,放出132.6kJ的热量,该方程式的∆H =。
(2)能判断该反应(在体积不变的密闭容器中进行)已经达到平衡状态的是()
A.焦炭的质量不再变化 B.N2和CO速率之比为1:3
C.生成6molCO同时消耗1mol Si3N4 D.混合气体的密度不再变化
(3)下列措施中可以促进平衡右移的是()
A.升高温度 B.降低压强 C.加入更多的SiO2 D.充入N2
(4)该反应的温度控制在1300-1700oC的原因是。
(5)某温度下,测得该反应中N2和CO各个时刻的浓度如下,求0—20 min内N2的平均反应速率,该温度下,反应的平衡常数K=。
| 时间/min |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
| N2浓度/mol·L-1 |
4.00 |
3.70 |
3.50 |
3.36 |
3.26 |
3.18 |
3.10 |
3.00 |
3.00 |
3.00 |
| CO浓度/mol·L-1 |
0.00 |
0.90 |
1.50 |
1.92 |
2.22 |
2.46 |
2.70 |