在酸性高锰酸钾溶液中加入过氧化钠粉末,溶液褪色,其中发生反应的离子方程式为:2MnO+16H++5Na2O2===2Mn2++5O2↑+8H2O+10Na+。下列判断正确的是
| A.O2是还原产物,Mn2+是氧化产物 |
| B.Na2O2既是氧化剂,又是还原剂 |
| C.标准状况下,产生22.4 L O2时反应转移2 mol e- |
| D.通常用浓盐酸酸化高锰酸钾溶液 |
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如右图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为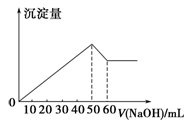
| A.6∶1 | B.3∶1 | C.2∶1 | D.1∶2 |
下列有关金属及其化合物的说法正确的是
| A.Mg和Al都可以用电解法冶炼得到 |
| B.Na2O和Na2O2与CO2反应产物相同 |
| C.MgO和Al2O3均只能与酸反应,不能与碱反应 |
| D.Mg和Fe在一定条件下与水反应都生成H2和对应的碱 |
Na2O2是一种既有氧化性、又有还原性的物质,当Na2O2与某物质Q发生反应并且有氧气生成时,下列有关说法正确的是
| A.Q一定是氧化剂 | B.当有1 mol O2生成时转移电子4 mol |
| C.O2一定是氧化产物 | D.Na2O2不可能发生还原反应 |
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
| A.将NaHCO3固体加入新制氯水,有无色气泡生成(H+) |
| B.使红色布条褪色(HClO) |
| C.向NaBr溶液中滴加氯水,再滴加CCl4,发现下层为橙红色(HCl) |
| D.滴加AgNO3溶液生成白色沉淀(Cl-) |
生活中常用氯气给自来水消毒。某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是
| A.石蕊 | B.硝酸银 | C.氢氧化钠 | D.氯化铝 |