下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是( )
| A.CH3CH2CH2CH3 | B.CH3CH(CH3)2 |
| C.CH3C(CH3)3 | D.(CH3)2CHCH2CH3 |
NM-3和D-58是正处于临床试验阶段的小分子抗癌药物,结构如下: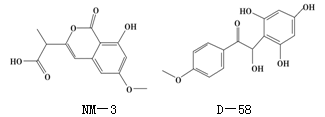
关于NM-3和D-58的叙述,错误的是()
| A.都能与NaOH溶液反应,原因不完全相同 |
| B.都能与溴水反应,原因不完全相同 |
| C.都不能发生消去反应,原因相同 |
| D.遇FeCl3溶液都显色,原因相同. |
褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。下列说法不正确的是()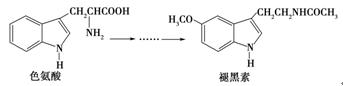
| A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点 |
| B.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出 |
| C.在一定条件下,色氨酸可发生缩聚反应 |
| D.褪黑素与色氨酸结构相似,也具有两性化合物的特性 |
下列各项中的两种物质无论以何种比例混合,只要混合物的总物质的量一定.则完全燃烧时生成水的质量和消耗O2的质量均不变的是()
| A.C3H6、C3H8O | B.CH4O、C2H4O3 |
| C.C2H2、C6H6 | D.C3H6、C2H6O |
分子式为C8H16O2的有机物A,能在酸性条件下水解生成B和C,且B在一定条件下能转化成C。则有机物A可能的结构有()
A.1种B.2种C.3种 D.4种
某有机物的结构简式如图所示,下列有关说法中不正确的是()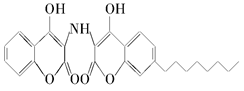
| A.分子式为C26H28O6N |
| B.遇FeCl3溶液不能发生显色反应 |
| C.1 mol该物质最多能与8 mol氢气发生加成反应 |
| D.1 mol该物质最多能与4 mol NaOH溶液完全反应 |