将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为( )
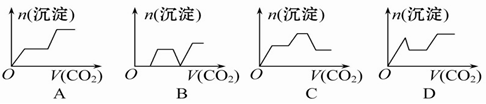
【2009届金溪一中、东乡一中高三第一次联考化学】有机物在酸性条件下发生水解反应时,生成两种不同有机物,且这两种有机物的相对分子质量相等。则水解前的这种有机物是( )
| A.甲酸甲酯 | B.乙酸异丙酯 | C.麦芽糖 | D.葡萄糖 |
某学生配制100mL1 mol·L-1的硫酸溶液,进行下列操作,然后对溶液浓度作精确测定,发现真实浓度小于1 mol·L-1,他的下列操作中使浓度偏低的原因是()
①用量筒量取浓硫酸时,俯视读数。
②量筒中浓硫酸全部转入烧杯中稀释后,再转移到1 00mL容量瓶中,烧杯未洗涤。
00mL容量瓶中,烧杯未洗涤。
③用玻璃棒引流,将溶液转移到容量瓶中有溶液流到了容量瓶外面。
④浓硫酸在小烧杯中稀释后,没有冷却就马上转移入容量瓶。
⑤用胶头滴管加蒸馏水时,加入过快而使液面超过了刻度线,立即用滴管吸去多余的水,使溶液凹面刚好与刻度线相切。
⑥滴加入蒸馏水,使溶液凹面刚好与刻度线相切,盖上瓶塞反复摇匀后,静置,发现液面比刻度线低,再加水至刻度线。
| A.②③④⑤⑥ | B.①②③⑤⑥ | C.②③⑤⑥ | D.①②③④⑤ |
今有0.1 mol·L-1 Na2SO4溶液300 mL,0.1 mol·L-1 MgSO4溶液200 mL和0.1 mol·L-1 Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子浓度之比是()
mL和0.1 mol·L-1 Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子浓度之比是()
| A.1∶1∶1 | B.3∶2∶2 | C.3∶2∶3 | D.1∶1∶3 |
下列叙述正确的是()
A.同温同压下,任何相同体积的物质 ,它们的物质的量必相等 ,它们的物质的量必相等 |
| B.任何条件下,等物质的量的二氧化碳和一氧化碳所含的分子数必相等 |
| C.1L二氧化碳气体一定比1L氮气的质量大 |
| D.等体积、等物质的量浓度的强酸中所含的H+数一定相等 |
V2O3和V2O5按不同的物质的量之比 混合,可按计量完全反应.今欲制备V8O17,则V2O3和V2O5的物质的量之比应为()
混合,可按计量完全反应.今欲制备V8O17,则V2O3和V2O5的物质的量之比应为()
| A.1∶2 | B.2∶1 | C.3∶5 | D.5∶3 |