下列离子方程式书写正确的是
| A.熔融状态下硫酸氢钾的电离方程式:KHSO4 = K++HSO4- |
B.NaHS水解:HS-+H2O H3O++S2- H3O++S2- |
| C.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+ =Fe3++3H2O |
D.碳酸电离:H2CO3 2H++CO32- 2H++CO32- |
反应2NO2(g) N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是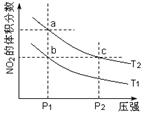
| A.a、c两点气体的颜色:a浅,c深 |
| B.a、c两点气体的平均相对分子质量:a>c |
| C.b、c两点的平衡常数:Kb=Kc |
| D.状态a通过升高温度可变成状态b |
模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示。下列说法正确的是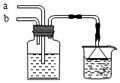
| A.a通入适量的CO2,b通入足量的NH3,纳米材料为Ca(HCO3)2 |
| B.a通入足量的NH3,b通入适量的CO2,纳米材料为Ca(HCO3)2 |
| C.a通入适量的CO2,b通入足量的NH3,纳米材料为CaCO3 |
| D.a通入少量的NH3,b通入足量的CO2,纳米材料为CaCO3 |
某未知溶液可能含Na+、NH4+、Fe2+、I-、Cl-、CO32-、SO32-。将该溶液加少量新制氯水,溶液变黄色。再向上述反应后溶液中加入BaCl2溶液或淀粉溶液,均无明显现象。下列推断合理的是
| A.一定存在Fe2+、Na+、Cl- | B.一定不存在I-、SO32- |
| C.一定呈碱性 | D.一定存在NH4+ |
在催化剂、400℃时可实现氯的循环利用,下图是其能量关系图,下列分析正确的是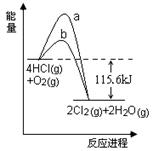
| A.曲线a是使用了催化剂的能量变化曲线 |
| B.反应物的总键能高于生成物的总键能 |
C.反应的热化学方程式为:4HCl(g) + O2(g) 2Cl2+2H2O(g)-115.6 kJ 2Cl2+2H2O(g)-115.6 kJ |
| D.若反应生成2mol液态水,放出的热量高于115.6kJ |
下列工业生产过程中涉及到反应热再利用的是
| A.接触法制硫酸 | B.联合法制纯碱 |
| C.铁矿石炼铁 | D.石油的裂化和裂解 |