沼气是一种能源,它的主要成分是CH4,0.5 mol CH4完全燃烧生成CO2和H2O(l)时,放出445 kJ热量,则下列热化学方程式正确的是
A.2CH4(g)+4O2(g) 2CO2(g)+4H2O(l) ΔH="+890" kJ· mol-1 2CO2(g)+4H2O(l) ΔH="+890" kJ· mol-1 |
B.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="+890" kJ· mol-1 CO2(g)+2H2O(l) ΔH="+890" kJ· mol-1 |
C.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="-890" kJ· mol-1 CO2(g)+2H2O(l) ΔH="-890" kJ· mol-1 |
D.1/2CH4(g)+O2(g) 1/2CO2(g)+H2O(l) ΔH="-890" kJ· mol-1 1/2CO2(g)+H2O(l) ΔH="-890" kJ· mol-1 |
根据陈述的知识,类推得出的结论正确的是
| A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O |
| B.NH3分子的空间构型是三角锥形;则BF3分子的空间构型也是三角锥形 |
| C.CO2和SiO2化学式相似,则CO2与SiO2的物理性质也相似 |
| D.第二周期元素氢化物稳定性顺序是HF >H2O >NH3;则第三周期元素氢化物稳定性顺序 |
也是HCl >H2S >PH3
在下面的电子结构中,属于P区的元素是
| A.2s2 | B.3d34s2 | C.3d104s2 | D.2s22p3 |
用分子间作用力的观点,下列最适合溶解硫粉(S8)的溶剂是
| A.水 | B.CH3OH(甲醇) | C.CS2 | D.CH3COOH(乙酸) |
下列叙述正确的是
| A.离子化合物中可能含有共价键 |
| B.原子晶体中的相邻原子间只存在非极性共价键 |
| C.分子晶体中的每个分子内一定含有共价键 |
| D.分子晶体常温下不可能为固态 |
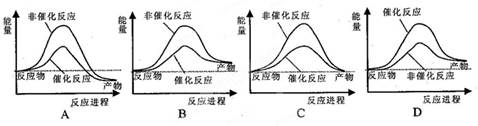
据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过的能量变化示意图正确的是