在100 ℃时,将0.40 mol二氧化氮气体充入2 L密闭容器中,每隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
| n(NO2)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
| n(N2O4)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
下列说法中正确的是
A.反应开始20 s内以二氧化氮表示的平均反应速率为0.001 25 mol·L-1·s-1
B.80 s时混合气体的颜色与60 s时相同,比40 s时的颜色深
C.80 s时向容器中加入0.32 mol氦气,同时将容器扩大为4 L,则平衡将不移动
D.若起始投料为0.20 mol N2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等
下列关于化学学科的认识说法不正确的是()
| A.化学模型是对事物及其变化的简单化模拟,有助于解释一些化学现象 |
| B.原子是化学变化中的最小微粒,通过复杂的化学反应可以产生新的元素 |
| C.有电子转移的过程不一定能产生电流,但其化学反应一定是氧化还原反应 |
| D.任何宏观物质都是由微观粒子构成,而这些粒子之间又存在着一定的作用力 |
A、B、C、D、E五种短周期元素,核电荷数依次增加。只有D为金属,A与D同主族,C与E同主族,B原子最外层电子数是内层电子数的2倍,D+与C3-具有相同的电子层结构。下列说法正确的是()
A.C的氧化物都能跟碱反应
B.B的最高价氧化物的水化物是非电解质
C.C的氢化物与C的最高价氧化物的水化物能发生化合反应
D.稳定性: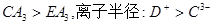
已知常温下: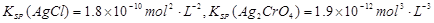 。则下列叙述正确的是()
。则下列叙述正确的是()
| A.AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小 |
B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明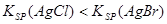 |
| C.将0.001mol·AgNO3溶液滴入0.001mol·L-1KCl和0.001mol·L-1K2CrO4混合溶液中,产生Ag2CrO4 |
| D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
在pH为4~5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。现欲除去溶液中的杂质离子,下述方法中可行的是()
| A.向溶液中加入纯Cu将Fe2+还原 |
| B.向溶液中通入H2S使Fe2+沉淀 |
| C.向溶液中通入Cl2,再通入CuO粉末调节pH为4~5 |
| D.向溶液中通入Cl2,再通入NH3调节pH为4~5 |
下列选项中所涉及到的两个量一定相等的是()
| A.36gH2O与1.204×1024个O2在标准状况下所占体积 |
| B.pH相等的氨水与醋酸溶液中由水电离出的OH-浓度 |
| C.pH相等的H2SO4和CH3COOH稀释相同倍数之后溶液的pH值 |
| D.等物质的量的Al分别与足量的盐酸、烧碱溶液反应转移的电子数 |