在不同温度下,水达到电离平衡时c(H+)与c(OH-)的关系如图所示,下列说法中正确的是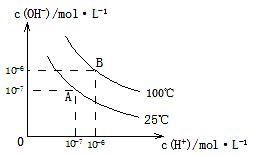
| A.100 ℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液等体积混合时恰好中和,所得溶液的pH等于7 |
| B.25 ℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/LHCl溶液等体积混合,所得溶液的pH等于7 |
| C.25 ℃时,0.2 mol/L NaOH溶液与0.2 mol/L醋酸等体积混合后恰好中和,所得溶液pH等于7 |
| D.25 ℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液的pH大于7 |
已知可逆反应2SO2+O2 2SO3是放热反应,下列说法正确的是
2SO3是放热反应,下列说法正确的是
| A.2molSO2 与1molO2 能完全反应生成2molSO3 ,升高温度可以加快此反应的化学反应速率 |
| B.2molSO2 与1molO2不能完全反应生成2molSO3,升高温度可以加快此反应的化学反应速率 |
| C.2molSO2 与1molO2 能完全反应生成2molSO3 ,升高温度减慢此反应的化学反应速率 |
| D.2molSO2 与1molO2 不能完全反应生成2molSO3 ,升高温度减慢此反应的化学反应速率 |
同一主族的X 、 Y 、 Z三种元素,已知最高价氧化物对应水化物的酸性强弱是H3XO4<H3YO4<H3ZO4 ,下列推断正确的是
| A.原子序数: X<Y<Z |
| B.气态氢化物稳定性: XH3>YH3>ZH3 |
| C.元素的非金属强弱: X>Y>Z |
| D.电子层数: X>Y>Z |
X元素的气态氢化物的化学式为H2X,则X的最高正价氧化物的对应的水化物的化学式为( )
| A.H2XO3 | B.X(OH)2 | C.H3XO4 | D.H2XO4 |
下列化合物中,阳离子半径与阴离子半径比值最小的是( )
| A.NaF | B.NaCl | C.MgI2 | D.KBr |
同主族元素形成的同一类型的化合物,往往结构和性质很相似,如PH4I的结构和性质与NH4Cl相似,有关对PH4I的叙述中不正确的是()
| A.可由PH3与HI化合生成 | B.将其加热可以分解 |
| C.能跟NaOH溶液反应 | D.是一种共价化合物 |