过氧化钙是一种安全无毒的物质,带有数量不等的结晶水,通常还含有部分CaO。
(1)称取0.542g过氧化钙样品,灼热时发生如下反应:2CaO2·XH2O  2CaO + O2↑ + 2XH2O,得到的O2在标准状况下体积为67.2mL,该样品中CaO2的物质的量为 。
2CaO + O2↑ + 2XH2O,得到的O2在标准状况下体积为67.2mL,该样品中CaO2的物质的量为 。
(2)另取同一样品0.542g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g。
① 试计算样品中CaO的质量。
② 试计算样品中CaO2·XH2O的X值。
反应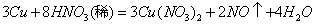 ,
,
(1)请用双线桥标出反应中电子转移的情况。
(2)若有19.2g Cu被氧化,则被还原的HNO3的质量为多少?
将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解,冷却后将混合液稀释至1000 mL,测得c(Cu2+)="0.3" mol/L。试计算:
(1)反应过程中放出的气体在标准状况下的体积(不考虑气体在溶液中的溶解)。
(2)溶液稀释后,c(H+)是多少?
把13 g含有SiO2的CaCO3固体在高温下加热到质量不再改变,冷却后称量为8.6 g则生成的CO2在标准状况下的体积为L,原混合物中含SiO2的质量g。
两种饱和一元醇A和B的分子中相差一个碳原子,现有A和B的混合物19.5 g与足量的钠反应生成了5.6 L H2(标准状况)。问A、B为何种物质?混合物中A、B的质量分数为多少?
一定量的某有机物与NaOH的醇溶液共热,产生的气体在标准状况下为896 mL,同时得溶液100 mL,取出10 mL溶液先用HNO3酸化后再加入AgNO3溶液直到不再产生白色沉淀为止,用去0.1 mol·L-1AgNO3溶液40 mL,所得气体完全燃烧时消耗O2 0.18 mol,试确定该有机物的结构简式和名称。