金属M在酸性或碱性溶液中均可与HNO3发生氧化还原反应,转化关系如下(部分生成物未列出):
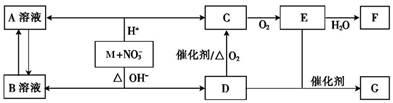
已知:C、D、E、G均为气体,且G为单质;将D通入A溶液产生白色沉淀;将F逐滴加入B溶液至过量,先产生白色沉淀,随后沉淀消失。
请回答下列问题:
(1)写出下列物质的化学式:M 、F 、G 。
(2)A溶液与B溶液混合也能产生白色沉淀,写出该反应的离子方程式 。 [
(3)除去气体C中的气体E的化学方法是 。
(4)将10mL充满气体E和O2混合气的试管倒扣在水槽中,反应后试管中残留1mL无色气体,则试管中气体E的体积是 mL。
(5)D →C反应的化学方程式是 。
(6)M与NO3-在碱性条件下反应的离子方程式为 。
反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
C(g)+D(g)过程中的能量变化如图所示,回答下列问题.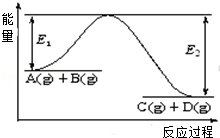
(1)该反应是 反应(填“吸热”、“放热”).
(2)当反应达到平衡时,升高温度,A的转化率 (填“增大”、“减小”、“不变”),原因是
(3)反应体系中加入催化剂对反应热是否有影响? (填“有”、“无”),原因是 .
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”、“减小”、“不变”).
将25℃ 101KPa条件下的氯化氢(HCl)气体49.6L,通入492mL水中,(已知水的密度为:1.00g/mL),得到密度为1.13g/mL的盐酸(即氯化氢的水溶液)。注:25℃101KPa条件下气体摩尔体积为24.8L/mol。
(1)此盐酸的质量分数为 (计算结果保留一位小数)
(2)此盐酸的物质的量浓度为 (计算结果保留一位小数)
(3)取出20.0 mL该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是 mL(计算结果保留一位小数)
(4)0.100 mol/L的稀盐酸500mL中含有的Cl-的数目为 (计算结果保留两位小数)
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________________mol。
(2)该气体所含原子总数为________________个。
(3)该气体在标准状况下的体积为_________________L。
(4)该气体在标准状况下的密度为_______________ g/L。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________________mol/L。
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)从氯化钠溶液中得到氯化钠固体,选择装置 (填代表装置图的字母,下同);除去自来水中的Cl﹣等杂质,选择装置 ;从碘水中分离出I2,选择装置 ,该分离方法的名称为 。
(2)装置A中①的名称是 ,冷却水的方向是______________,温度计水银球的位置是在 ;装置B在分液时装置中的液体不能顺利滴下,原因是______________________。
(3)从碘水中得到碘时,不能选用的试剂是____________
A.酒精 B.苯 C.四氯化碳
若选则试剂X(密度小于水的密度)从碘水中提取碘时,充分振荡、静置后,下层液体的颜色为 。
有科学家正在研究用碳与一氧化氮反应处理环境问题:
C(s)+2NO(g)⇌CO2(g)+N2(g)△H
(1)实验方案中有下列措施①采用加热提高反应速率②使用催化剂提高反应速率③使用加压提高NO转化率④使CO2转化成干冰从体系用脱离,提高NO的转化率其中你认为可行的是 .
(2)这个反应的平衡常数表达式是 .
(3)在恒容恒温密闭容器中,科学家得到下列实验数据:
浓度(mol/L)
时间(min) NO N2 CO2
0 0.100 00
10 0.058 0.0210.021
20 0.040 0.0300.030
30 0.0400.030 0.030
请求出该应在该温度下的平衡常数K= .
(4)若在(3)的实验中30min时开始升温,36min时达平衡,测得NO的转化率变为50%,则该反应的△H 0(填“>”、“<”、“=”),判断的理由是 .
(5)若科学家在30min后改变了某一条件,反应进行到40min时达平衡浓度分别为C(NO)=0.032mol/L,C(N2)=0.034mol/L,C(CO2)=0.017mol/L,则改变的条件可能是 ,判断的依据是 .