下列反应的离子方程式正确的是
| A.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3↓+H+ |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+= Fe3++3H2O |
| C.向含有0.4 mol FeBr2溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br﹣+3Cl2= 4Fe3++6Cl﹣+Br2 |
D.用Pt电极电解饱和氯化镁溶液:2Cl﹣+2H2O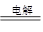 H2↑+Cl2↑+2OH﹣ H2↑+Cl2↑+2OH﹣ |
丙烯酸的结构简式为CH2=CH—COOH,其对应的性质中不正确的是()
| A.与钠反应放出氢气 | B.与碳酸氢钠反应 |
| C.能与溴水发生取代反应 | D.发生相互加成反应生成高分子化合物 |
下列物质既能发生消去反应生成相应的烯烃,不能氧化生成相应醛的是 ( )
| A.CH3OH | B.CH3CH2CH2OH | C.CH3CCH2OH | D.CH3CHCH3 |
已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,分别为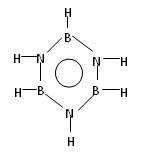

硼氮苯的二氯取代物(B3N3H4Cl2)的同分异构体的数目为( )
| A.2 | B.3 | C.4 | D.5 |
下列有机物命名正确的是 ( )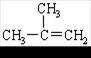
A. 2-乙基丙烷 2-乙基丙烷 |
B.CH3CH2CH2CH2OH 1-丁醇 |
C.CH3- -CH3间二甲苯 -CH3间二甲苯 |
D.2-甲基-2-丙烯 |
下列通式只表示一类物质的是( )
| A.CnH2n+2 | B.CnH2n | C.CnH2n-2 | D.CnH2n-6 |