利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)  5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通人4 molCO,测得CO2的体积分数随时间t变化曲线如图。请回答:
5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通人4 molCO,测得CO2的体积分数随时间t变化曲线如图。请回答:
(1)T2时,0~0.5min内的反应速率v(CO)=___________。
(2)T1时化学平衡常数K=______________。
(3)下列说法不正确的是_______(填字母序号)。
| A.容器内气体密度不变,表明反应达到平衡状态 |
| B.两种温度下,C点时体系中混合气体的压强相等 |
| C.d点时,增大体系压强,CO的转化率不变 |
| D.b点和d点时化学平衡常数的大小关系:Kb<Kd |
将蔗糖溶于水配成10%的溶液,分装在两个试管中.在第一个试管中加入几滴稀硫酸并水浴加热,然后再加入新制的Cu(OH)2并加热,没有红色沉淀产生,原因是__________________________________;在第二个试管中加入几滴稀硫酸,再放在水浴中加热,再加入足量的NaOH溶液并加入新制的Cu(OH)2,加热后的现象是______________________,加入足量NaOH溶液的作用是______________________.上述实验中发生反应的化学方程式是__________________________________________.
在葡萄糖溶液中有一种环状结构的葡萄糖分子,化学式是C6H12O6,在溶液中存在下列平衡: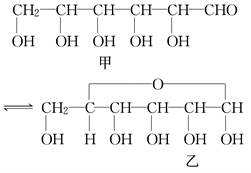
(1)上述平衡中的环状结构乙的分子是通过链状结构甲分子的________基和________基之间发生________反应而生成的.
(2)现要制备一种链羟基醚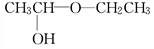 ,试写出由两种简单的有机物合
,试写出由两种简单的有机物合
成该羟基醚的化学方程式为
________________________________________________________________________.
科学家预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂作用水解成葡萄糖,再将葡萄糖转化为乙醇,用作燃料.
(1)写出绿色植物的秸秆转化为乙醇的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________.
(2)乙醇还可用于合成其他有机物,如图是用乙醇为起始原料合成环状酯D的框图,请在方框内填入相应有机物的结构简式: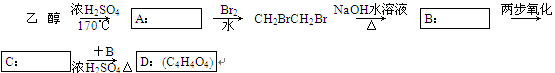
(3)写出B+C―→D的化学方程式:________________________________________
_______________________________________________________________________.
分别取1 mol葡萄糖进行下列试验:
(1)银镜反应时,生成Ag的物质的量为________ mol,反应后葡萄糖变为________,其结构简式是______________________________.
(2)与乙酸反应生成酯,从理论上讲完全酯化需要________ g乙酸.
(3)若使之完全转化为CO2和H2O,所需氧气的体积在标准状况下为________ L,反应的化学方程式是________________________________.
据新华社2009年5月9日电, 国务院总理温家宝主持召开国务院常务会议,会上通过了我国2009年将投入大量资金发展新能源汽车,支持节能、环保、安全等关键技术开发,为我国社会经济可持续发展打下良好基础,为今后改善环境、提升民众的生活质量具有极为重要的意义。请回答下列问题:
(1)氢能是理想的清洁能源,也是氢氧燃料电池的必不可少的物质。请回答下列问题。
①下列说法不正确的是。
A.太阳光催化分解水制氢比电解水制氢更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH为介质的氢氧燃料电池负极电极反应相同
D.氢氧燃料电池正极获得8mol电子,负极需要8g气体
②利用MnFe2O4为催化剂,通过两步反应使水分解制氢气,第一步反反应为:
MnFe2O4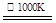 MnFe2O4-X+(X/2)O2
MnFe2O4-X+(X/2)O2
则第二步反应的化学方程式为(条件不写)。
③一种新能源汽车,使用了以碳纳米管为储氢介质的燃料电池,电池原理如右图,该电池的电解质为6mol/LKOH溶液,下列说法不正确的是。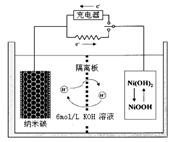
A.放电过程中整个体系内KOH浓度不变
B.放电时负极附近pH减小
C.放电时电池正极的电极反应为:NiO(OH)+H2O+e—=Ni(OH)2+OH—
D.放电时,电池反应为2H2+O2→2H2O
(2)热值指在一定条件下每克物质完全燃烧所放出的热量(燃烧产物在该条件下是一种较为稳定的状态),下表是几种物质在常温常压下的热值数据。已知:管道煤气(47g/m3H2、625g/m3CO)价格为1.00元/m3,天然气(714g/m3CH4)的价格为2.50元/m3。
| 物质 |
H2 |
CO |
CH4 |
| 热值/kJ·g–1 |
143 |
10 |
56 |
①根据以上热值数据,是最理想的燃料。
②家庭使用管道煤气和天然气, 更经济合算。
③表示CO燃烧热的热化学方程式为 。